

文 | 徐佳琳 畢業于加拿大英屬哥倫比亞大學;
馬培敏 畢業于美國普度大學。
兩位均供職于某藥企臨床藥理部門。本文僅代表個人觀點,與所在公司無關。
太長不看版:
瑞德西韋治療新冠病毒的臨床試驗已經啟動。
在當前缺藥的情況下,重新啟動瑞德西韋這樣的藥物是緊急情況下“老藥新用”的合理嘗試,但面臨巨大挑戰和風險。
臨床試驗設計中的瑞德西韋劑量已經接近安全劑量的上限,但能達到的體內濃度依然低于體外測試時抑制病毒所需濃度。
戰略性儲備盡量多的廣譜抗病毒藥物,才可能避免在未來疫情中再次陷入目前無藥可用的困境。
自新冠肺炎爆發以來,“藥物臨床試驗”這個名詞頻頻進入公眾的視野。從1月底到2月10日,中國研究者們已注冊了81項相關的臨床試驗,各式各樣的都有。
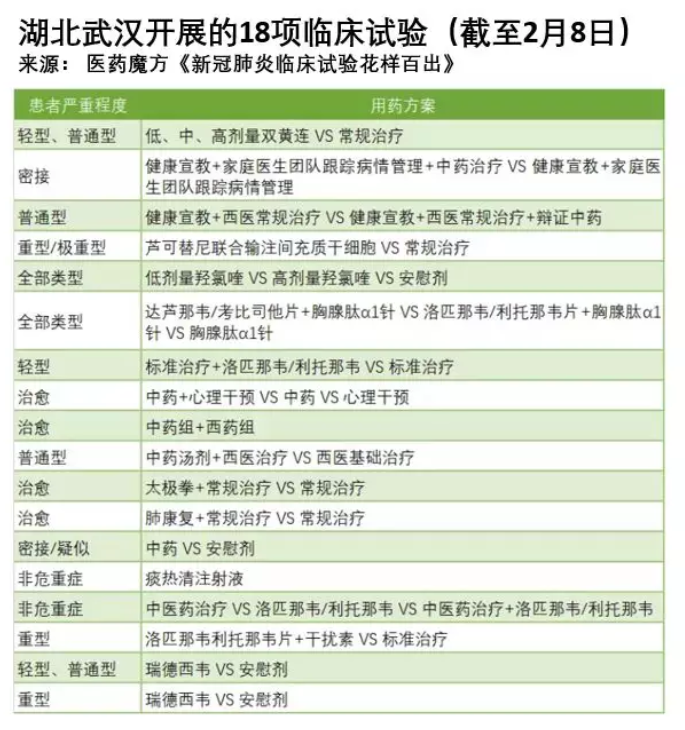
圖片來自與網頁截圖
在各類藥物和療法信息中,以瑞德西韋最為耀眼,被不少媒體和公眾號譽為“特效藥”、“神藥”。
瑞德西韋治療新冠病毒感染的臨床試驗,已于2月5 日啟動(ClinicalTrials.gov編號:NCT04252664及NCT04257656)。大家可能知道,這個藥物幾年前在抗埃博拉病毒的臨床試驗中失敗了,那這次它有多大希望成功呢?
每個人都有自己的看法,我們想從臨床藥理學角度,解析和討論使用瑞德西韋治療新冠肺炎臨床試驗的可能理由及用藥方案。
臨床藥理學:連接臨床前體外實驗、動物實驗和人體臨床確證性試驗的專門學科,也是制訂和指導藥物的臨床用法用量的主要工具。
瑞德西韋能抑制新冠病毒么?
2017年,吉利德公司的科學家們發現,他們正在開發的抗埃博拉病毒藥物瑞德西韋對包括SARS、MERS等人類冠狀病毒以及多種蝙蝠攜帶的冠狀病毒都具有活性。
在用人類呼吸道上皮細胞做的體外實驗中,瑞德西韋對SARS和MERS病毒的EC50分別為0.069和0.074μM(微摩爾每升)。
EC50是衡量藥物抑制病毒活性的一個濃度指標,一般來講,這個數值越小,說明抑制病毒的能力越強。
在這個基礎上,中科院武漢病毒所對新冠病毒做了類似研究:在來源于腎臟的上皮細胞中,瑞德西韋對新冠病毒的EC50為0.77μM,數值看起來比抑制SARS等病毒的能力低了近10倍。
誠然,兩次試驗結果不能直接比較,因為來自不同實驗室,試驗用了不同類型細胞(人類呼吸道vs 猿猴腎臟)。但數值提示我們:瑞德西韋對新冠病毒有體外活性,但抑制能力可能不如對SARS和MERS病毒的強。
另外,目前還沒有新冠病毒的動物模型驗證過瑞德西韋對新冠病毒具有體內活性。
瑞德西韋能達到需要的劑量么?
藥物的判斷標準,包括了療效和副作用。一個理想的抗病毒藥物,應當能抑制體內病毒,又不會或很少產生不良反應。
要判斷一個藥物對人體的潛在療效或安全性,通常是從體外實驗或動物實驗的數據來推論。其中最關鍵的數據之一,就是藥物濃度。
當實驗藥物進入臨床試驗時,先要了解的就是它在人體內達到的實際濃度。
瑞德西韋很特殊,它需要進入細胞內部被轉換為活性代謝物(代號GS-443902),才能發揮抑制病毒的作用。2018年發布的早期臨床試驗報告中,29名健康人使用瑞德西韋后,體內血漿藥物和PBMC中活性代謝物的平均濃度如下:
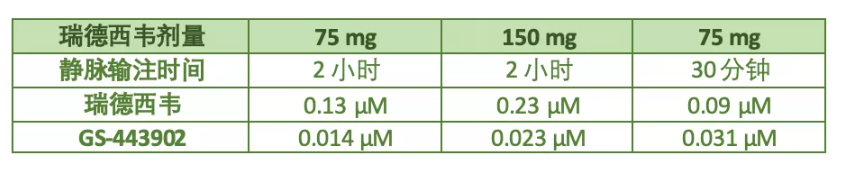
注:數據經藥代動力學計算與單位轉換
從這個表格中,可以看到:
1)藥物劑量與瑞德西韋及其活性代謝物的濃度大體成比例;
2)靜脈輸注時間越短,細胞內藥物有效成分(GS-443902)的濃度越高。
按照我們查閱的數據,這次瑞德西韋治療新冠病毒感染的臨床試驗中的試驗劑量為第1天200mg,第2-10天每天100mg。
我們先看看瑞德西韋能達到抑制病毒需要的濃度么?
假設采取30分鐘靜脈勻速輸注給藥,可以粗略推算出體內平均濃度為0.12μM,比武漢病毒所測得的EC50要低很多。如果想要人體中的濃度超過武漢病毒所測出的體外EC50(0.77μM),則需要提高劑量到每天至少650mg(假設在增加劑量時,瑞德西韋體內濃度按比例增加)。
即使藥物在人體的平均濃度達到EC50,距離藥物臨床有效仍有距離。EC50只是實驗室環境里抑制50%的病毒增長所需的濃度,而實際也許需要抑制人體內90%甚至更多病毒增長。
然后我們看看安全風險。
埃博拉的臨床試驗發現,在每天用藥的情況下,多名使用150mg藥物的健康人出現了輕度肝功能損傷,目前臨床中已知的瑞德西韋最高單次安全劑量是225mg。因此,目前在中國開展的這兩項臨床試驗中使用的瑞德西韋劑量已接近安全劑量的上限。
還值得一提的是,在體外細胞試驗中,瑞德西韋抑制埃博拉病毒的EC50值介于0.06-0.14μM之間,對應活性代謝物約5μM,看起來比抑制新冠病毒的能力更強。即便如此,在2019年的抗埃博拉病毒三期臨床試驗中,瑞德西韋失敗了,遠不如同一研究中使用的其他兩種藥物,從此瑞德西韋被吉利德公司打入冷宮。
雖然我們內心都希望能盡快出現新藥,但從藥理方面的數據推導,目前瑞德西韋的試驗劑量想要在人體內產生抑制新冠病毒的效應,非常困難。
“決定做”到“怎么做”,還要考慮哪些問題?
新藥研發從來都不是一蹴而就的,從驗證藥物的體外活性,到動物體內活性、安全性,再到人體內的安全性和有效性研究,需要循序漸進,耗時多年。
非典爆發17年以后,目前尚無藥物可有效治療SARS或MERS等冠狀病毒感染。
在當前缺藥的情況下,重新考慮瑞德西韋這樣的藥物是緊急情況下“老藥新用”的合理嘗試,立即開展臨床試驗不失為一種快捷方法。
但是知易行難,“決定做”相對容易,想清楚“怎么做”和“做什么”就更困難,而后兩者也是達成最終目標所必需的。
決定“怎么做”,就包括從臨床藥理的角度理性分析已有數據去幫助更好地設計試驗。
值得考慮的臨床藥理因素包括種族差異、藥物在人體內的劑量與濃度、藥效/安全性的定量關系,藥物適用人群等。另外,靜脈輸注時間為何會影響瑞德西韋及其活性代謝物濃度?藥物是否存在肝臟蓄積?等等問題也是需要回答的。
除了做臨床試驗外,使用臨床同情用藥、制定建立藥物有效性計劃、設定嚴謹的數據庫以準備相應的數據分析等,也應該作為真實世界證據研究的做法被考慮。
面對病毒,我們將何去何從?
自從生命誕生以來,人類與病毒導致的傳染病對抗從未停歇:從1918年奪去幾千萬條生命的西班牙流感,到2003年的SARS,及本次新冠病毒等。長期存在于蝙蝠中的冠狀病毒對它們無害,大多數情況下也不會感染人類。從宏觀上,人類與動物、細菌、病毒等共同生存甚至互相依賴,所以我們熱愛和珍惜的不應僅是人類的性命,還應敬畏其他動物生命,尊重大自然。
關于新冠病毒本身,許多問題需要繼續研究:流行病學數據及傳播方式,易感人群(老人或免疫功能較低、其他基礎疾病患者等);迄今為止,新冠病毒的原始宿主(蝙蝠?)和可能的中間宿主(穿山甲?)尚未定論,意味著人們還難以從根本源頭控制傳染。
在和平時期,戰略性儲備盡量多的廣譜抗病毒藥物,才可能避免在未來疫情中再次陷入目前無藥可用的困境。
新型傳染病的大規模爆發有如懸在頭上的達摩克利斯之劍:問題不是這樣的事件是否會發生,而是什么時候發生。
當傳染病再次來襲時,人類能否從容應對?
寫在最后
疫情之下,作為科研工作者,我們能做和想做的,是以臨床藥理學為工具,幫助篩選、評估和開發有臨床潛力的新老藥物,為抗擊新冠肺炎盡綿薄之力。
相信在舉國守望相助、共克時艱的努力下,疫情終將得到紓解,也希望在一線英勇奮斗的醫療工作者能平安回家。
致謝:感謝孫雪瑩、李宗益對本文中的學術問題提出寶貴意見和建議。
來源:微信公眾號“菠蘿因子” (ID:checkpoint_1)
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn