- 首頁
- 資訊
海正藥業獲“法匹拉韋”藥品注冊批件和臨床試驗批件
來源:海正藥業 2020-02-17
導讀:近日,浙江海正藥業股份有限公司收到國家藥品監督管理局核準簽發的法維拉韋片(又稱:法匹拉韋片) 的《藥品注冊批件》和《藥物臨床試驗批件》。《藥物臨床試驗批件》顯示該藥物適應癥為新型冠狀病毒肺炎。

2月17日,海正藥業發布公告稱其獲得法維拉韋片(又稱:法匹拉韋片) 的《藥品注冊批件》和《藥物臨床試驗批件》。《藥物臨床試驗批件》顯示該藥物適應癥為新型冠狀病毒肺炎。
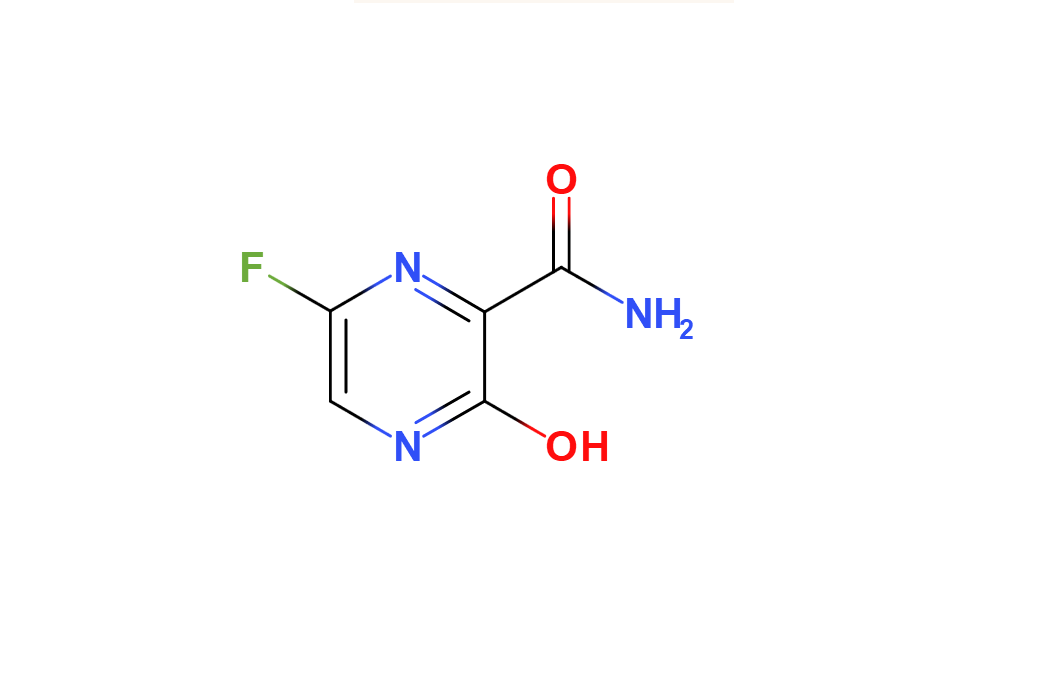
審批結論:根據《藥品管理法》、《藥品注冊管理辦法》等,經審查,本品基本符合審批的有關規定,附條件批準生產本品(上市后要求繼續完成尚未完成 的藥學方面和臨床藥理方面相關研究,完成后向國家藥品審評機構及時報送研究結果),同時發給藥品批準文號。本品生產工藝、質量標準、說明書和包裝標簽, 及原料藥生產工藝、質量標準和包裝標簽按所附執行。 適應癥:用于治療成人新型或再次流行的流感(僅限于其它抗流感病毒藥物 治療無效或效果不佳時使用)。 審批結論:根據《藥品管理法》、《藥品注冊管理辦法》和《藥品特別審批 程序》,經特別專家組評議審核,應急批準本品進行臨床試驗。適應癥為新型冠狀病毒肺炎。 法維拉韋片(又稱:法匹拉韋片)于2014年3月獲批在日本上市,為廣譜抗病毒藥物,適應癥為用于治療成人新型或再次流行的流感(僅限于其它抗流感病毒藥物治療無效或效果不佳時使用)。富山化學工業株式會社于1999年8月對法匹拉韋進行了最早的化合物專利申請,期限20年。海正藥業與日本富山化學工業株式會社在2016年6月簽定了化合物專利獨家授權協議。該化合物專利已于2019年8月到期,海正藥業研發生產該藥品符合相關規定。此前海正藥業該藥品未實現商業化生產。經查詢 IMS 數據庫,未查詢到該品種在國內外市場的銷量數據。截至目前,海正藥業在法維拉韋研發項目上已投入約 4,003 萬元。
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn