

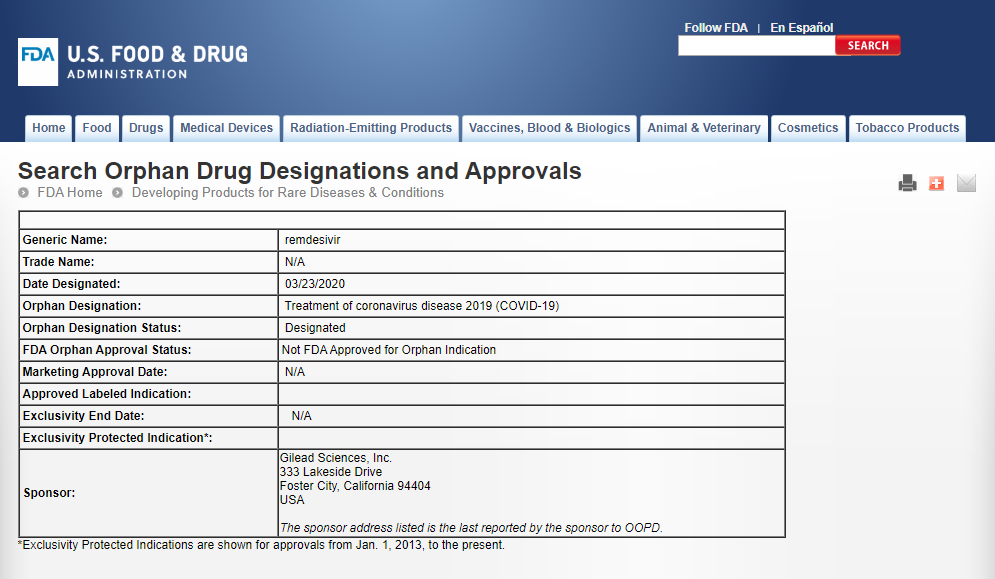
3月23日,FDA官網數據庫顯示,FDA授予吉利德科學(Gilead Sciences)公司開發的在研抗病毒療法瑞德西韋(remdesivir)孤兒藥資格(Orphan Drug Designation),其適應癥為冠狀病毒疾病2019(COVID-19)。
瑞德西韋是一種在研的核苷酸類似物,具有廣譜抗病毒活性,在體外和體內動物模型中顯示了對多種新興病毒病原體的活性,包括埃博拉病毒、馬爾堡病毒、中東呼吸綜合征(MERS)和非典型性肺炎(SARS)病毒。針對瑞德西韋的研究曾在健康志愿者和埃博拉病毒感染者中展開。個別同情用藥病例不足以確定瑞德西韋治療新型冠狀病毒肺炎的安全性和有效性,這只能通過未來的臨床試驗來確定。
孤兒藥本是指一些專門用于治愈或治療/控制罕見病的藥物。罕見疾病的定義是在美國是患病人數小于20萬人(或發病人口比例000)的疾病。通常,罕見病藥物的研發成本高昂,上市之后價格也高昂,但企業回報卻未必豐厚。從而在追求利潤和投資回報的情況下,醫藥企業不重視針對適用癥或適用病患過少的罕見疾病進行研發。為了鼓勵對被忽視的罕見病治療用藥研發,1983年開始美國FDA給針對孤兒癥的研究項目提供綠色通道,加速審批的過程。同時,孤兒藥身份可以為制藥公司提供在該是適應癥上為期7年的市場獨占期(排他性),即7年內任何藥廠不得仿制該藥物用于在獲批適應癥領域進行治療。在藥物開發過程中,制藥企業還能夠獲得與合格臨床測試相關的稅務抵免,以及交付新藥申請時特定費用的減免等其他優惠。
吉利德科學公司開發的瑞德西韋近來成為大家關注的熱點藥物。它是一款抗病毒療法,其作用機制為抑制RNA依賴性RNA聚合酶的活性,從而抑制RNA病毒的增殖。目前,吉利德公司正在進展6項臨床試驗,檢驗瑞德西韋治療不同類型的COVID-19患者的療效。其中,在中國進行的兩項臨床試驗有望在4月獲得結果。
為了滿足可能出現的未來需求,該公司已經擴大瑞德西韋的生產能力,并且將生產兩種瑞德西韋的配方(液體和凍干)。該公司表示,目前正在將提供個人同情使用(compassionate use)緊急通道過渡到擴展使用項目(expanded access programs),這種方法將加速重癥患者獲得瑞德西韋的機會,并能夠收集所有參與患者的數據。這些項目目前正在與全球各國監管機構聯合快速開發。
太平洋時間2020年2月26日,吉利德科學宣布啟動兩項三期臨床研究,以評估瑞德西韋在治療新型冠狀病毒肺炎成人患者中的安全性和有效性。從今年3月開始,這兩項隨機、開放、多中心的研究將主要在亞洲以及全球其他確診病例較多的國家的醫療中心展開,入組約1,000名患者。研究將評估瑞德西韋靜脈給藥的兩種用藥時間方案。吉利德就使用瑞德西韋治療新型冠狀病毒肺炎提出了研究申請(IND),美國食品藥品監督管理局(FDA)在迅速審評后,批準吉利德啟動這些臨床試驗。
新的臨床研究擴展了正在進行中的針對瑞德西韋的研究,這其中包括在中國湖北省開展的由中日友好醫院負責的兩項臨床試驗,以及最近在美國由國家過敏和傳染病研究所(NIAID)主導的一項臨床試驗。吉利德為這些研究捐贈了藥品并提供科學支持,在中國的臨床試驗預計四月份獲得結果。
兩項研究中的第一項將通過靜脈注射5天和10天的給藥方案來評估瑞德西韋的安全性和有效性。大約400名重度癥狀患者將按照1:1的比例被隨機分配,除標準治療之外,他們會在第一天接受靜脈注射瑞德西韋200 mg,此后每天注射瑞德西韋100 mg,直到第5天或第10天。本研究的主要目的是通過衡量體溫和氧飽和度的正常化來評估瑞德西韋的療效(即:腋下溫度< 36.6 度,口腔溫度< 37.2 度,肛溫< 37.8度;血氧飽和度 > 94%,持續至少24小時,直到第14天)。
第二項研究將評估瑞德西韋靜脈給藥5天和10天的方案對新型冠狀病毒肺炎中度癥狀患者的安全性和有效性,并與單純接受標準治療的患者進行比較。大約600名參與者將按照1:1:1的比例隨機分組,除標準治療之外,患者第一天接受瑞德西韋200 mg治療,此后每天注射瑞德西韋100 mg,直到第5天或第10天,把他們與單獨接受標準治療的參與者做比較。本研究的主要目的是通過衡量每組患者在第14天時的出院人數比例來評估瑞德西韋的療效。
“吉利德的首要關注點是迅速確定瑞德西韋作為新型冠狀病毒肺炎潛在治療方案的安全性和有效性。這些互補的研究有助于幫助我們在短時間內獲得關于此藥物的更廣泛的全球性數據。瑞德西韋針對冠狀病毒的研究得以快速開展,反映了探尋疾病治療方案的緊迫性以及制藥業、政府、全球衛生機構和醫療人員共同應對這一公共衛生挑戰的高度使命感,”吉利德科學首席醫療官Merdad Parsey博士表示。
吉利德發起的臨床試驗將對瑞德西韋的兩種給藥時間方案進行評估。一項研究將入組約400名臨床表現嚴重的新型冠狀病毒肺炎患者,隨機分配讓他們接受5天或10天的瑞德西韋治療。第二項研究將在約600名具有中度臨床癥狀的患者中展開,隨機分配讓他們接受5天或10天的瑞德西韋治療或者僅接受標準治療。兩項研究的主要終點是臨床癥狀的改善,詳細描述請見文末。
瑞德西韋尚未在全球任何國家獲得許可或批準,其安全性和有效性尚未被證實。除了進行中的臨床試驗之外,吉利德正與政府機構、非政府組織和地方監管部門合作,為符合條件的新型冠狀病毒肺炎患者提供同情用藥緊急治療。

2月1日,吉利德科學全球首席醫療官Merdad Parsey博士代表公司發布聲明,稱吉利德正與全球的衛生機構密切合作,提供在研藥物Remdesivir(瑞德西韋)用于試驗性治療,以支持應對新型冠狀病毒(2019-nCoV)感染的暴發。
2月2日,中日友好醫院宣布其在武漢疫區牽頭開展瑞德西韋(Remdesivir)治療2019-nCoV新型冠狀病毒臨床研究,為抗擊疫情帶來曙光。
2月4日,中國科學院武漢病毒研究所發布其開展聯合研究,在抑制2019新型冠狀病毒(2019-nCoV)藥物篩選方面取得重要進展。相關研究成果以“Remdesivir and chloroquine effectively inhibit the recently emerged novel coronavirus (2019-nCoV) in vitro”(《瑞得西韋和磷酸氯喹能在體外有效抑制新型冠狀病毒(2019-nCoV)》)為題發表在中國自主知識產權的國際知名學術期刊Cell Research(《細胞研究》)上。該研究表明,在Vero E6細胞上,瑞得西韋(Remdesivir, GS-5734)對2019-nCoV的半數有效濃度EC50=0.77 uM(微摩爾每升),選擇指數SI大于129;磷酸氯喹(Chloroquine)的EC50=1.13 uM,SI大于88,說明上述兩種藥物在細胞水平上能有效抑制2019-nCoV的感染,其在人體上的作用還有待臨床驗證。
2月5日,武漢市金銀潭醫院召開科技部應急攻關“瑞德西韋治療2019新型冠狀病毒感染研究”項目啟動會,會上介紹瑞德西韋(remdesivir)已完成臨床試驗的注冊審批工作,第一批病例入組工作也已就位。首批新型冠狀病毒感染的肺炎重癥患者2月6日將接受用藥。瑞德西韋臨床試驗由中日友好醫院、中國醫學科學院藥物研究所牽頭,研究將在武漢金銀潭醫院等多家臨床一線接診新型冠狀病毒感染肺炎患者的醫院中進行,擬入組761例患者,采用隨機、雙盲、安慰劑對照方法展開。
2月7日,重慶博騰制藥科技股份有限公司發布公告,稱已收到核心客戶 Gilead Sciences, Inc.(吉利德科學)在研抗病毒藥物 Remdesivir(瑞德西韋) 的中間體訂單確認函件。
2月12日,博瑞醫藥發布公告稱,憑借其在高端原料藥和特殊注射劑開發領域的技術積累,該公司成功開發了瑞德西韋原料藥合成工藝技術和制劑技術,并已經批量生產出瑞德西韋原料藥,瑞德西韋制劑批量化生產正在進行中。
2月25日,國務院聯防聯控機制舉行新聞發布會,國家知識產權局副局長何志敏介紹,瑞德西韋臨床試驗正在進行中,4月27日才能公布臨床試驗的結果。圍繞瑞德西韋,吉利德科學公司的確在中國申請了8件專利,目前已經有3件專利得到授權,還有5件正在審查的過程中。這8件專利申請的保護范圍涵蓋了化合物的核心結構和類似結構以及晶型,以及相關的制造方法、用途等等。
2月26日,吉利德科學宣布啟動兩項三期臨床研究,以評估瑞德西韋在治療新型冠狀病毒肺炎成人患者中的安全性和有效性。
3月23日,美國食品和藥品管理局(FDA)官網數據庫顯示,FDA授予吉利德科學(Gilead Sciences)公司開發的在研抗病毒療法瑞德西韋(remdesivir)孤兒藥資格(Orphan Drug Designation),其適應癥為冠狀病毒疾病2019(COVID-19)。
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn