



(圖片來源:J. Am. Chem. Soc.)
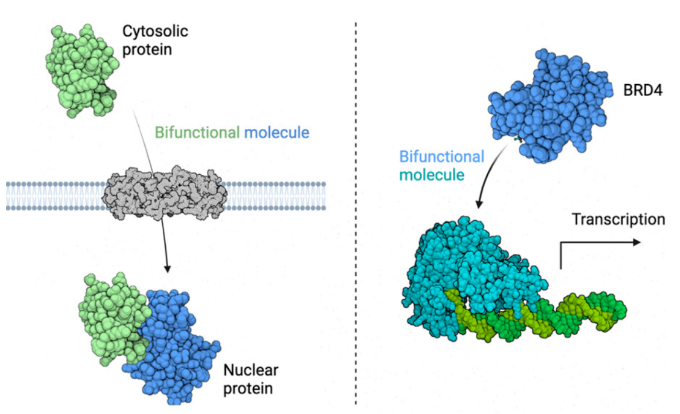
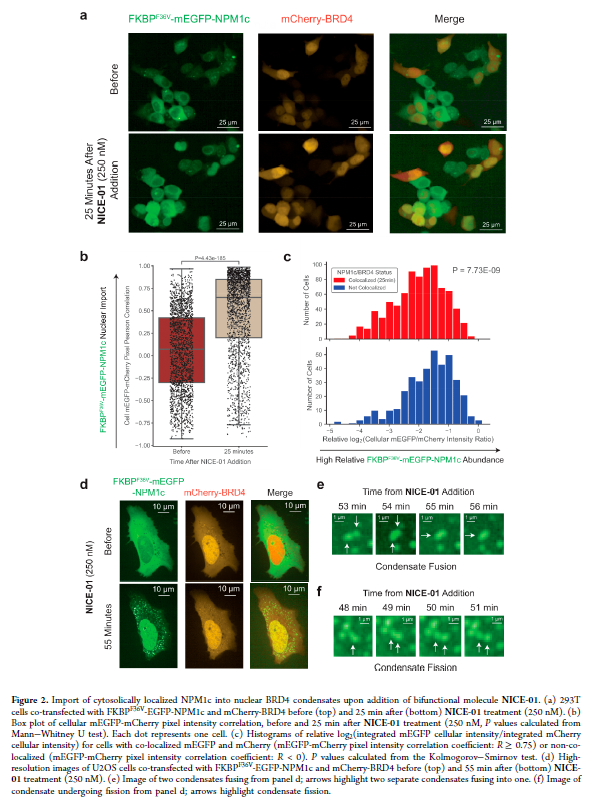
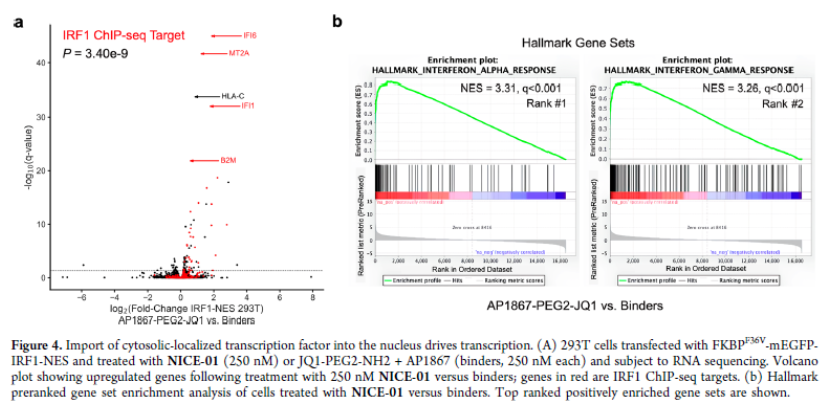
正文 細胞被劃分為不同的隔間,以調(diào)節(jié)信息流并聚集生物分子。在真核細胞中,有兩個主要的區(qū)室:細胞質(zhì)和細胞核。最近的研究進一步強調(diào)了蛋白質(zhì)空間定位的重要性,蛋白質(zhì)在細胞中的異常定位是各種疾病發(fā)展的關(guān)鍵因素。為了更好地理解并潛在地操縱蛋白質(zhì)定位以治療各種相關(guān)疾病,作者設(shè)計了一種雙功能分子來達到上述目的。下載化學加APP到你手機,更加方便,更多收獲。 首先,作者假設(shè)化學誘導靶蛋白與組成性核蛋白的接近將實現(xiàn)靶蛋白核定位(圖1a)。為了證實這一點,作者選取了一種豐富的、核定位的且具有經(jīng)過充分驗證的、可以功能化的小分子結(jié)合劑的蛋白質(zhì)——BET溴結(jié)構(gòu)域蛋白,并以JQ1為其配體,合成了由JQ1和AP1867組成的雙功能分子(NICE-01,圖1b),AP1867用來結(jié)合FKBPF36V。隨后作者發(fā)現(xiàn),在FKBPF36V-mEGFP和mCherry-BRD4共轉(zhuǎn)染的細胞中添加NICE-01(200 nM,40分鐘;圖1c)后FKBPF36V-EGFP快速易位到細胞核。然后,作者假設(shè)內(nèi)源性含BET的蛋白質(zhì)可以用作核導入的“載體”。在穩(wěn)定表達FKBPF36V-mEGFP的細胞中,NICE-01(250 nM,3小時)可以在細胞核中富集mEGFP(圖1d和圖S1)。 雙功能化合物的一個決定性特征是觀察到“鉤效應(yīng)”(hook effect)。在缺乏外源mCherry-BRD4的細胞中,10 μM NICE-01不能誘導FKBPF36V-mEGFP的入核。然而,在該劑量下轉(zhuǎn)染mCherry-BRD4能夠讓入核發(fā)生(圖1f)。這與理論一致,即在給定濃度的化合物下,三元復(fù)合物形成的減少可以通過進一步添加蛋白質(zhì)來緩解。 (圖片來源:J. Am. Chem. Soc.) 隨后,作者還發(fā)現(xiàn),三元復(fù)合物組分的化學計量是影響核導入的關(guān)鍵。當依賴于內(nèi)源性BET蛋白時,F(xiàn)KBPF36V-mEGFP的入核程度較弱,缺乏mEGFP胞質(zhì)排斥(圖1g和圖S1),這可能與通過瞬時轉(zhuǎn)染獲得的蛋白水平異常高于內(nèi)源性蛋白水平有關(guān)。這一結(jié)果表明,核導入的細胞特異性一部分表現(xiàn)在核定位載體表達的數(shù)量差異。另外,配體親和力似乎也很重要。 (圖片來源:J. Am. Chem. Soc.) 接下來,作者假設(shè)可以使用化合物處理后觀察到的FKBPF36V-mEGFP濃度的變化來計算蛋白質(zhì)在核膜中擴散的動力學參數(shù)并構(gòu)建了一個核導入步驟的模型(圖S3)。對單個細胞的胞質(zhì)FKBPF36V-mEGFP的部分進行定量。在短的初始期后,核輸入相對于細胞質(zhì)中的FKBPF36V-mEGFP部分顯示出一級動力學(圖S3)。這個估算的結(jié)果接近HeLa細胞中麥芽糖結(jié)合蛋白的被動輸入速率。這些數(shù)據(jù)表明,結(jié)合BRD4的雙功能化合物誘導靶蛋白封閉在核內(nèi)。 (圖片來源:J. Am. Chem. Soc.) 先前的研究表明,將細胞質(zhì)突變體NPM1c重新定位到細胞核中可以減少HOX基因的表達,從而誘導白血病分化和細胞死亡。用FKBPF36V-mEGFP-NPM1c和mCherry-BRD4共轉(zhuǎn)染的細胞在用NICE-01處理后幾分鐘內(nèi)顯示FKBPF36V-mEGFP-NPM1c快速重新定位到細胞核中(圖2a)。 (圖片來源:J. Am. Chem. Soc.) 有趣的是,并不是所有的細胞對化合物處理都表現(xiàn)出一致的反應(yīng)。作者分析了導入程度不同的細胞的FKBPF36V-EGFP-NPM1c與mCherry-BRD4的比率(圖2c)。數(shù)據(jù)表明,三元復(fù)合物組分的化學計量可以影響對雙功能化合物的表型反應(yīng),并可以解釋觀察到的單細胞表型異質(zhì)性。 作者用雙功能化合物處理NPM1c和BRD4共轉(zhuǎn)染的U2OS細胞,然后每1分鐘進行一次高分辨率顯微鏡成像,證實了胞質(zhì)和核仁凝聚物中的NPM1c移動到BRD4凝聚物中(圖2d)。作者還注意到FKBPF36V-mEGFP摻入核凝聚物中,即使它們依賴于內(nèi)源性含BET的蛋白質(zhì)入核(圖1e)。這些發(fā)現(xiàn)表明,鄰近誘導分子可以針對性地改變凝聚物的組成。 隨后,作者假設(shè)p53能夠作為核載體來誘導NPM1c在細胞核中的定位。用FKBPF36V-mEGFP-NPM1c和Halo-p53R273H-mCherry轉(zhuǎn)染293T細胞,令人驚訝的是, Halo-p53R273H-mCherri僅在與FKBPF36V-mEGFP-NPM1c共轉(zhuǎn)染時定位于細胞質(zhì)(圖3a)。 (圖片來源:J. Am. Chem. Soc.) 細胞溶質(zhì)p53與DNA在物理上分離,其大部分腫瘤抑制活性可能受到抑制。因此,NPM1c介導的p53出核可能對突變的致癌性至關(guān)重要,這一點尚不清楚。作者發(fā)現(xiàn)NICE-01并不能在表達BRD4 Flag和FKBPF36V-mEGFP-NPM1c的293T細胞中重新定位Halo-p53R273H-mCherry,這表明p53并不總是以一定的共定位方式與NPM1c在物理上連接(圖3e)。 (圖片來源:J. Am. Chem. Soc.) 最后,作者認為NICE-01可以誘導轉(zhuǎn)錄因子IRF1的核導入和轉(zhuǎn)錄激活。在不存在雙功能化合物的情況下,F(xiàn)KBPF36V-mEGFP-IRF1-NES從細胞核中移出(圖S4)。當用NICE-01(250 nM)處理時,在共表達mCherry-BRD4和FKBPF36V-mEGFP-IRF1-NES的細胞中可以觀察到mEGFP快速導入(<20分鐘)。然而,在沒有外源性BRD4的情況下,作者無法通過光學顯微鏡檢測到FKBPF36V-mEGFP-IRF1-NES的輸入,這可能是因為與BRD4相比,F(xiàn)KBPF36V-mEGFP-IRF1-NES大大過量(圖S4)。在用NICE-01(250 nM)處理并表達FKBPF36V-mEGFP-IRF1-NES的293T細胞中,RNA-seq顯著上調(diào)IRF1-ChIP-seq靶點(圖4a)。通過基因集富集分析,作者還觀察到標志性干擾素反應(yīng)基因集的顯著陽性富集(圖4b)。這些結(jié)果表明化學誘導BRD4定位于胞質(zhì)轉(zhuǎn)錄因子足以誘導其靶基因的表達。 (圖片來源:J. Am. Chem. Soc.) 總結(jié)




聲明:化學加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權(quán)益,請作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn