

(圖片來源:Nat. Chem.)
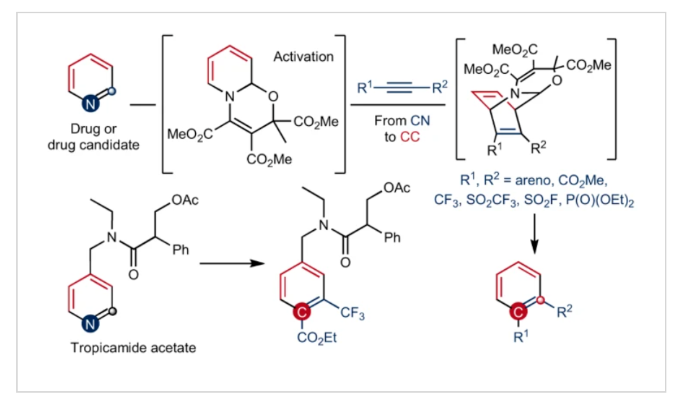
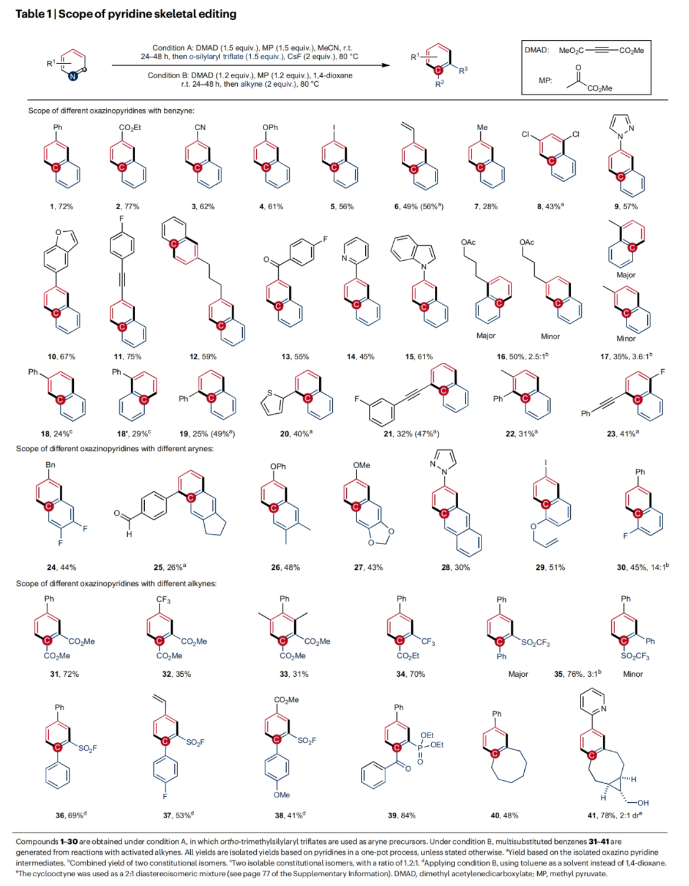
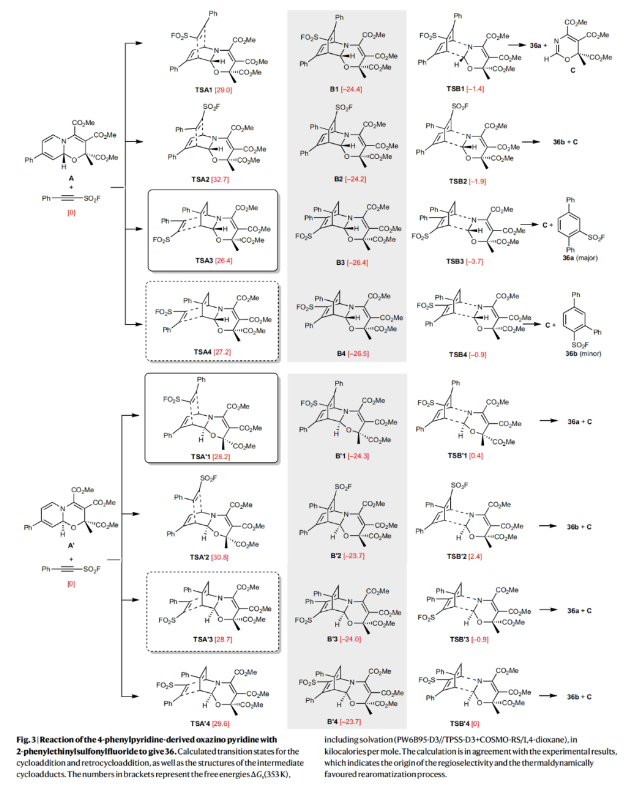
正文 骨架編輯是合成化學中最直接的合成策略,其可以將復雜分子的核心結構中的原子進行精確取代或重排。此外,它還可以使化合物實現快速多樣化,這是通過其它編輯策略所不能實現的。目前已報道的芳烴骨架編輯策略主要依賴于卡賓或乃春類型的插入反應或重排發生的。雖然這些高效策略可以適用于雜芳烴結構的后期修飾,但卻不能應用于吡啶的骨架編輯。最近,德國明斯特大學(Universit?t Münster)Armido Studer課題組報道了通過CN到CC的原子對交換策略,以模塊化的方式實現了吡啶的骨架編輯,構建了一系列多取代的苯和萘。下載化學加APP到你手機,更加方便,更多收獲。 作者所發展的骨架編輯策略依賴于在環加成反應中作為富電子二烯的oxazino吡啶的反應活性。重要的是,此類oxazino吡啶是穩定的化合物,其很容易利用吡啶作為原料來大規模制備。在[4+2]環加成反應中,二烯胺中間體作為雙烯體,親電的炔或芳炔作為親雙烯體。得到的橋聯環加合物將進行再芳構化的逆環加成反應,形成穩定的苯或萘。包括吡啶的初始去芳構化在內,整個過程可以在一鍋內呈現,通過CN與CC原子對的交換直接將吡啶接轉化為苯或萘(Fig. 1)。 (圖片來源:Nat. Chem.) 通過對最優反應條件進行探索,作者發現此過程在無需使用催化劑的條件下,僅在乙腈或1,4-二氧六環中80 oC加熱即可實現,且整個體系對空氣和濕度均不敏感。隨后,作者探索了此策略的底物兼容性(Table 1)。實驗結果表明,一系列不同取代的吡啶和苯炔均具有良好的兼容性,以24-77%的產率得到相應的萘產物1-30。其中包括芳基碘在內的基團均可兼容(5),這為產物的后續衍生化提供了多種可能性。除此之外,一系列對稱與非對稱的炔烴也可以作為親雙烯體參與轉化,以41-72%的產率,良好的區域選擇性得到相應的取代苯產物31-41。因此,此原子對交換策略可以為從吡啶構建多取代苯提供一種直接的合成方法。 為了證明開發的吡啶骨架編輯策略的應用潛力,作者將此反應應用于藥物及其衍生物的后期修飾(Fig. 2a)。以酰基保護的tropicamide為例(42-45),其吡啶骨架可以與不同的親雙烯體通過一鍋法骨架編輯得到不同的苯和萘衍生物。此外,loratadine (46)的內部雙鍵和蛋白激酶抑制劑(protein kinase inhibitor)(51)的噻吩環均耐受性良好。通過對吡啶-stanolone (47,49)、吡啶-indomethacin (48)和吡啶-estron (53)進行簡單的衍生化,作者可以使用此原子交換策略在分子內引入醫學和農業化學相關的官能團,如羧酸鹽、膦酸鹽和三氟甲氧基等。此外,由于該方法可模塊化合成,作者還可以通過將藥物轉化為親雙烯體來進行修飾。Probenecid衍生的炔烴可以在吡啶編輯反應中作為環加成反應試劑,以88%的產率得到膦酸鹽和吡唑結合的苯衍生物50。同樣地,對于(+)-δ-tocopherol衍生的芳炔前體,通過與取代吡啶反應可以得到相應的取代萘衍生物,盡管形成了兩個構造異構體(52,54)。此外,為了證明該方法在藥物化學和工藝化學中的應用性,作者還實現了兩種不同藥物和藥物衍生物的克級規模一鍋吡啶編輯反應(46,47)。實驗結果表明兩個反應均順利進行,在放大規模后不會影響產率,即使與stanolone衍生物的反應也是可以在空氣氛圍下進行的(47)。 接下來,當作者利用芳基噻蒽鎓鹽55作為芳炔前體時,可以以48%的產率得到相應的萘產物56。此外,一鍋法策略同樣可行,以32%的產率得到56(Fig. 2b)。 最后,作者通過DFT計算對此[4+2]環加成反應以及隨后的逆環加成反應進行了探索(Fig. 3)。起始oxazino吡啶的兩個非對映異構體(A和A’)僅相差0.6 kcal mol-1,這說明了為什么兩個異構體都是在初始去芳構化步驟中形成的(比例為4:1)。在與非對稱炔烴的[4+2]環加成反應中,可能存在8種不同的過渡態,作者對所有過渡態均進行了計算。且計算結果與實驗所觀察到的結果基本一致,盡管實驗比理論預測的區域選擇性略低。 (圖片來源:Nat. Chem.) 總結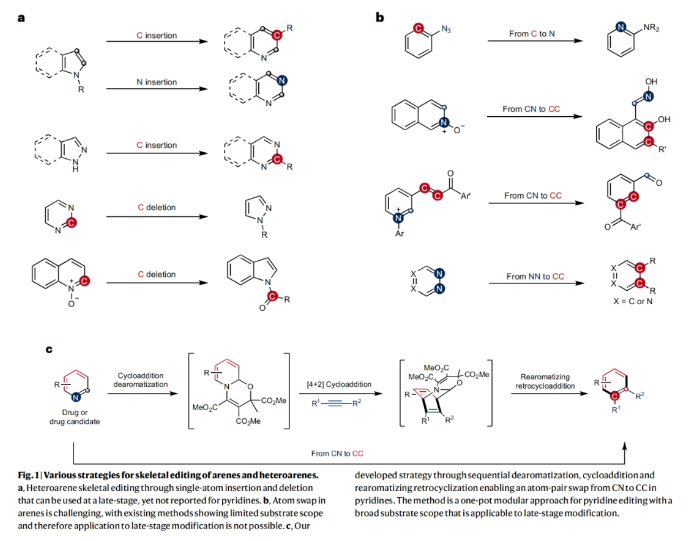

聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn