

苝醌化合物被認為是光動力療法中理想的光敏劑之一。然而,天然的苝醌化合物具有光穩定性差、暗毒性高以及無選擇性的缺點。為了發掘具有優異特性的苝醌化合物,江南大學饒義劍團隊基于B類苝醌化合物的分支代謝途徑,采用合成生物學策略對尾孢菌素的生物合成途徑進行重編程,實現了一系列具有不同構型和取代基苝醌衍生物的生物合成。其中,非天然苝醌化合物尾孢菌甲素(cercosporin A)不僅具有較高的光穩定性和極低的暗毒性,并且保留了良好的光動力抑菌和抗癌活性。此外,研究發現尾孢菌甲素可以選擇性地在細胞中富集,為苝醌化合物的藥物開發提供了潛在的靶點,并拓寬了從自然界中發現藥物的渠道。
首先,作者以實驗室分離保存的尾孢菌素高產菌株Cercosporasp. JNU001為研究對象,通過基因敲除、體外重構以及生物信息學分析揭示了B類苝醌天然產物由共同前體經分支酶的修飾形成產物多樣性和復雜性的機制,然后以尾孢菌素生物合成基因簇為模板,通過分支酶的敲除和引入獲得了一系列重編程的基因簇,不僅實現了苝醌化合物軸手性的改造,還獲得了一系列具有不同取代基的非天然苝醌化合物。此外,作者對關鍵分支酶的底物混雜性進行了詳細的測試,為其他非天然苝醌化合物的定向生物合成提供指導。
隨后,作者選取了幾種具有典型結構的天然或非天然苝醌化合物,從光物理學性質、單線態氧量子產率以及生物活性等方面考察了苝醌的化學結構對其光動力學特性的影響。結果表明,具有特殊骨架結構的苝醌化合物19在紅光區的吸收明顯增強;此外,與天然苝醌化合物相比,非天然苝醌化合物尾孢菌甲素不僅具有較高的光穩定性和顯著降低的暗毒性,還保留了良好的光動力抑菌和抗癌活性。
為了探究非天然苝醌化合物尾孢菌甲素暗毒性降低的原因,作者首先分析了不同苝醌化合物在細胞表面分布的差異。不同于尾孢菌素在細胞上的均勻分布,非天然苝醌化合物尾孢菌甲素在細胞表面呈選擇性富集;同時,細胞凋亡、DNA氧化損傷以及脂質氧化水平分析表明,在黑暗條件下尾孢菌甲素僅產生微量的活性氧成分,因此具有較低的暗毒性。
綜上所述,饒義劍教授團隊利用合成生物學方法對天然的尾孢菌素生物合成途徑進行重編程,獲得了優于自然的非天然苝醌化合物,解決了目前天然苝醌化合物光穩定性差、暗毒性高以及無選擇性等問題,為苝醌化合物的藥物開發奠定了堅實的基礎。
上述工作在線發表在Angewandte Chemie International Edition,饒義劍教授為該論文的通訊作者,江南大學博士生蘇增平和郭保黨為該論文的共同第一作者。上述研究工作得到了國家重點研發計劃(2018YFA0901700),國家自然科學基金(32270082),江蘇省自然科學基金(BK20202002)和江蘇省研究生科研與實踐創新項目(KYCX21_2020)等基金資助。
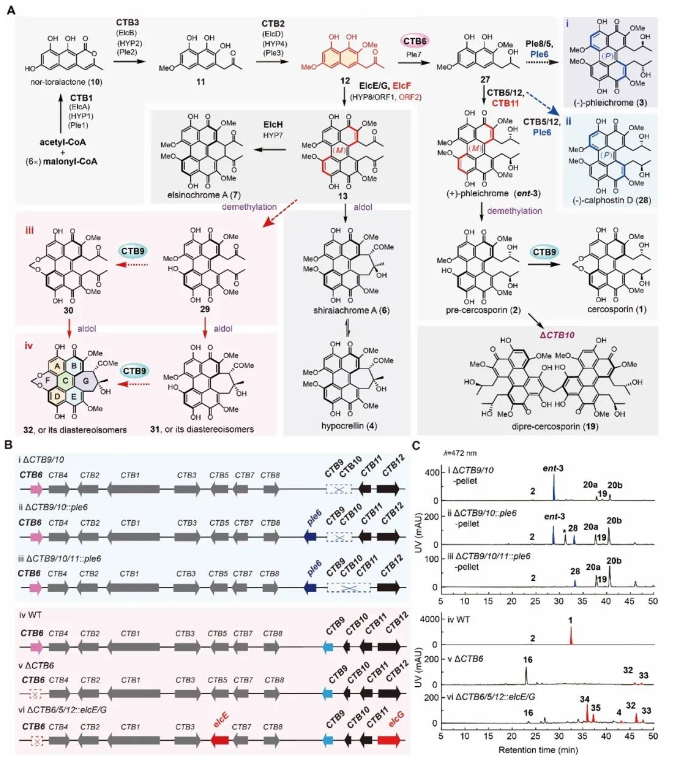
非天然苝醌化合物的設計與生物合成
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn