

為了解決這一問題,近日美國加州大學洛杉磯分校段鑲鋒教授和Philippe Sautet教授等人合作,以氮、硫、雙摻雜多孔石墨烯框架(N, S-HGF)電催化劑和未摻雜的HGF作為對比研究對象。并通過多種表征手段建立了詳細的反應網絡,闡明了中心中間體Li2S4前后的主要反應途徑,識別了關鍵中間相,如Li2S4和Li2S,并確定了非電化學比例在Li2S8和Li2S4之間的重要性。此外,通過對比N, S-HGF和HGF,作者驗證了N, S-HGF催化劑能夠加速LiPSs的轉化,使其在較高電位下更快耗盡,從而緩解了多硫化物的穿梭效應,提高了電池的輸出性能。這項研究為理解電催化SRR機理提供了重要的見解,并為設計更高效的催化劑提供了理論指導。

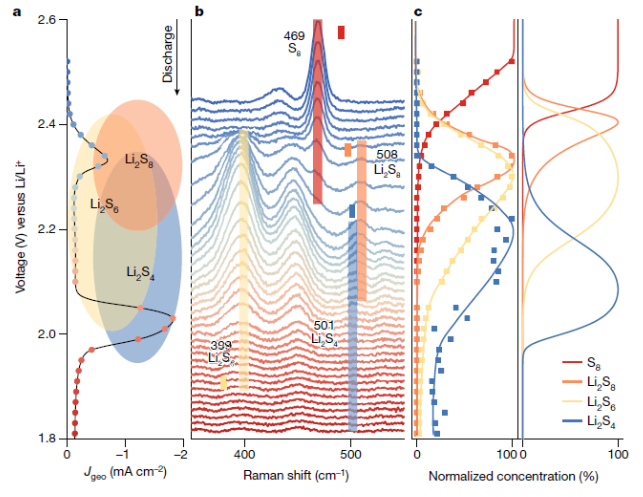
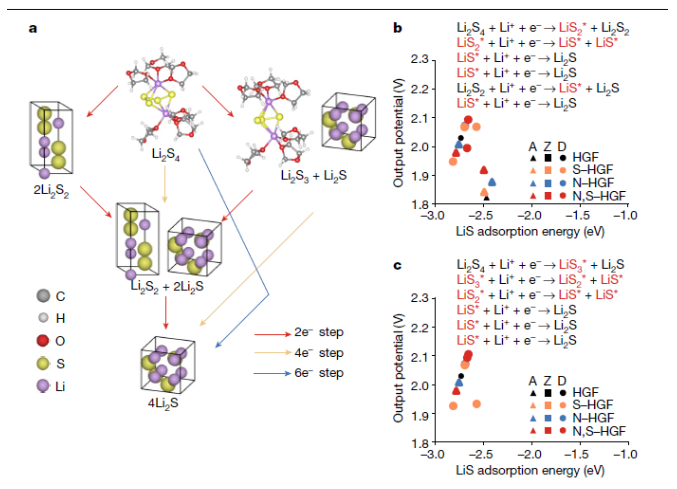
正文 為了讓讀者形象理解鋰硫電池中涉及的多硫化物轉化反應,作者在圖1a展示了該電池中涉及的SRR的示意圖。其中,SRR涉及從S8分子到Li2S固體的復雜的16電子轉化過程。圖1b顯示了具有N,S–HGF催化劑的CV曲線。插圖顯示了在約2.11–2.25 V的近似電壓范圍內的平臺,這是Li2S8轉化為Li2S4的延遲引起的電壓變化范圍。圖1c示意了本研究中使用的原位拉曼技術。總之,圖1形象的給讀者展示了一個微觀化學原子反應的機理,有助于作者進一步采用一些表征手段去驗證這個想法。下載化學加APP到你手機,收獲更多商業合作機會。。 圖片來源:Nature 為進一步揭示N,S–HGF對Li-S電池中多硫化物轉化反應的顯著影響(圖2)。作者首先確認了N,S–HGF相較于未摻雜的HGF能夠明顯加速SRR動力學。比如通過對CV曲線進行積分,計算得到的電荷數被轉換為完整的16電子過程中的電子轉移數。在第二個峰值(2.11 V)開始處分離整體放電過程,得到了一個電荷轉移比為4.08:11.92(約等于1:3),這一比例經過電流-放電測試進行驗證。這表明Li2S4是主要中間體分隔了兩個還原峰。為了探究這一反應的化學起源,作者使用第一性原理計算了不同多硫化物中間體之間的基本能量學。計算模擬顯示,從S8到Li2S8的轉化產生了2.41 V的最高計算輸出電位。而Li2S8分子的進一步轉化涉及多個可能的分支,計算表明形成兩個Li2S4的路徑是放熱比較嚴重的,所以是最有可能產生2.24 V的輸出電位。最后,考慮到實驗中觀察到的平臺可能源于混合反應產物的延遲電化學轉化,作者通過將DFT計算結果與電壓效應結合,模擬得到不同多硫化物的濃度隨電位的變化。計算顯示,主導的LiPS相的順序為S8、Li2S8、Li2S6、Li2S4和Li2S。從濃度導出的CV曲線得到的電荷比為2.82:1.20:11.98,與實驗中觀察到的比例相匹配。這一研究為理解Li-S電池中復雜的反應機制提供了重要的依據,為優化電池性能提供了理論指導。 圖2. SRR的電荷分析和反應網絡。 為了探究Li-S電池放電過程中的具體反應中間體,作者采用了原位拉曼光譜技術對放電CV掃描過程中的反應中間體進行了研究。圖3a,b展示了在不同電位下反應中間體的變化。結果表明,在初始狀態下存在典型的S8峰(469 cm?1),證實了元素硫的存在。隨著電位的降低,S8信號逐漸減小,并在約2.36 V處消失,同時約2.44 V下出現了Li2S8信號(508 cm?1)并伴隨著Li2S6峰(399 cm?1)的出現。隨后,Li2S8峰值逐漸減小,而Li2S4峰(501 cm?1)在約2.18 V時達到最大值。隨著電位的降低,Li2S4成為主要的多硫化物,而通過共晶反應形成的Li2S6也顯著存在。通過比較實驗和計算結果,發現了S8、Li2S8、Li2S6、Li2S4在不同電位下的濃度變化具有相似的序列。值得注意的是,Li2S6的出現電位與Li2S8相似,而其消耗電位與Li2S4相似,表明通過共晶/非共晶反應之間存在動態平衡。這些結果有助于更好地理解Li-S電池的放電機制,并為設計更高性能的電池提供了重要參考。 圖片來源:Nature 為了進一步了解電催化劑對SRR的影響,作者對比研究了非摻雜的HGF與N,S–HGF的催化系統(圖4)。結果顯示,在高電位處這兩種不同催化劑的放電第一步在某種程度上存在差異。具體是Li2S8的峰在HGF中稍有延遲。此外,Li2S6的轉化對非摻雜的HGF更為敏感。這是因為在這種情況下Li2S4的轉化動力學較慢,從而延遲了低價態的多硫化物消耗,使其出現在更低的電位區域(低于1.97 V),但是在該區域中電化學還原Li2S6也可能開始發生。所以結果說明Li2S4的轉化主導了電催化過程,特別是在SRR的第二階段開始時。這些CV和實時拉曼研究顯示了HGF和N,S–HGF之間明顯的SRR動力學差異,突顯了高效催化劑帶來的好處。 圖4. SRR中不同催化劑的比較。 圖5通過研究第二階段的反應途徑——即從Li2S4到Li2S的轉化,以了解這兩種電催化劑的不同電位范圍。考慮從Li2S4開始的所有可能的電子轉移步驟(見圖5),他們在各種催化劑位點的存在下檢查了總共12種不同的反應途徑。結果發現了兩個產生最高輸出電位的途徑(見圖5c)。比如,在這兩個途徑中,相對于非摻雜位點為2.03 V ,N,S共摻雜位點表現出更高的輸出電位(2.11 V),因此展示了N,S–HGF的卓越性能。有趣的是,內部缺陷位點在輸出電位圖中位于頂部的距離較近(圖5b、c),與花邊和鋸齒邊緣位點(分別為三角形和方形)相比,驗證了石墨烯摻雜對電催化的有效性。這表明,最終從Li2S2到Li2S的轉化是電位限制的步驟。HGF和N,S–HGF有效輸出電位的模擬差異僅在第二階段顯著,與實驗結果基本相符。實驗證明和理論之間的這種密切關聯進一步驗證了改進Li-S電池的電催化策略。 總結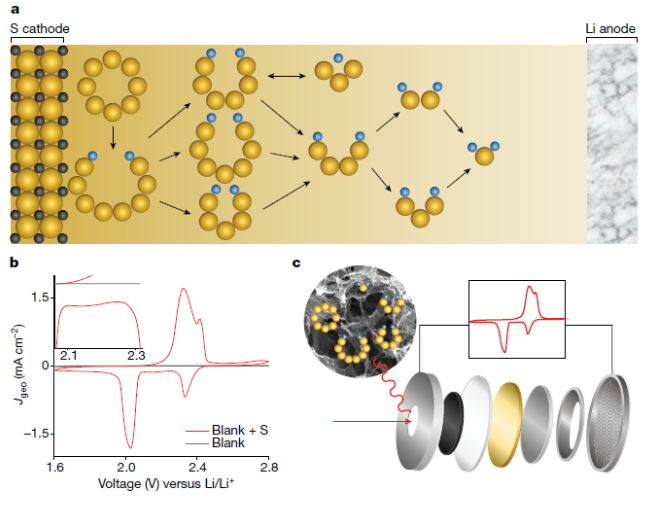


聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn