

將氟原子或含氟片段引入藥物分子,能夠有效地改變藥物分子的pKa、脂溶性、代謝穩定性以及滲透性,影響藥物分子的吸收、分布和代謝。因此,向藥物分子中引入“氟”已經成為藥物開發中非常重要的一部分,逐步成為藥物篩選的一種常用手段。2021年美國FDA批準的小分子藥物中,30%都是有機氟化合物。目前,超過25%的藥物都是有機氟化合物。制藥工業對含氟化合物的高需求極大地推動了有機氟化學的發展,越來越多的化學合成方法被應用于制備含氟分子,藥物開發中的含氟分子數量劇增。
與之相反,自然界中含氟分子的數量卻十分有限。到目前為止,人們僅發現約30種天然有機氟化合物,但是同為鹵素家族的天然有機氯化合物和有機溴化合物有近2000種已被發現。導致自然界中有機氟化合物稀缺的一個重要原因是酶促碳–氟鍵形成機制的單一性,目前唯一已知能夠在生物合成途徑中催化C–F鍵形成的酶是氟化酶(Fluorinase),它能夠催化氟負離子親核進攻S-腺苷甲硫氨酸(SAM)產生5'-氟脫氧腺苷(5'-FDA)。但是,自然界進化產生的氯化酶和溴化酶可以利用多種反應機制來構建碳–鹵鍵,如:經歷次氯酸根中間體的親電鹵代機制、經歷鐵氧中間體的自由基鹵代機制以及親核鹵代機制(圖1)。
目前,通過酶促反應合成有機氟化合物的研究,主要集中在拓展氟化酶的底物范圍以及將含氟砌塊引入代謝途徑這兩大策略,盡管已經取得了一定進展,但是酶催化C–F鍵形成的發展仍顯不足。如何建立新的生物催化機制來構建C–F鍵仍然是酶催化領域中頗具挑戰性的科學難題。鑒于此,研究團隊近日共同報道了基于新催化機制的酶促不對稱氟化反應,首次將自由基氟原子轉移機制引入到單一金屬酶催化體系,實現了高立體選擇性的氟轉移過程(圖2)。
本文研究團隊建立了一種能夠介導不對稱氟原子轉移反應的酶催化體系。這項工作證明非血紅素鐵酶中的鐵–氟中間體能夠與碳自由基反應生成碳–氟鍵,這也預示著其它的非血紅素鐵酶有望參與自由基型的氟轉移反應,能夠用于開發非天然途徑的氟化反應。該工作為非血紅素鐵酶的進一步工程化改造提供了借鑒,也為酶促氟化反應提供了新的思路。
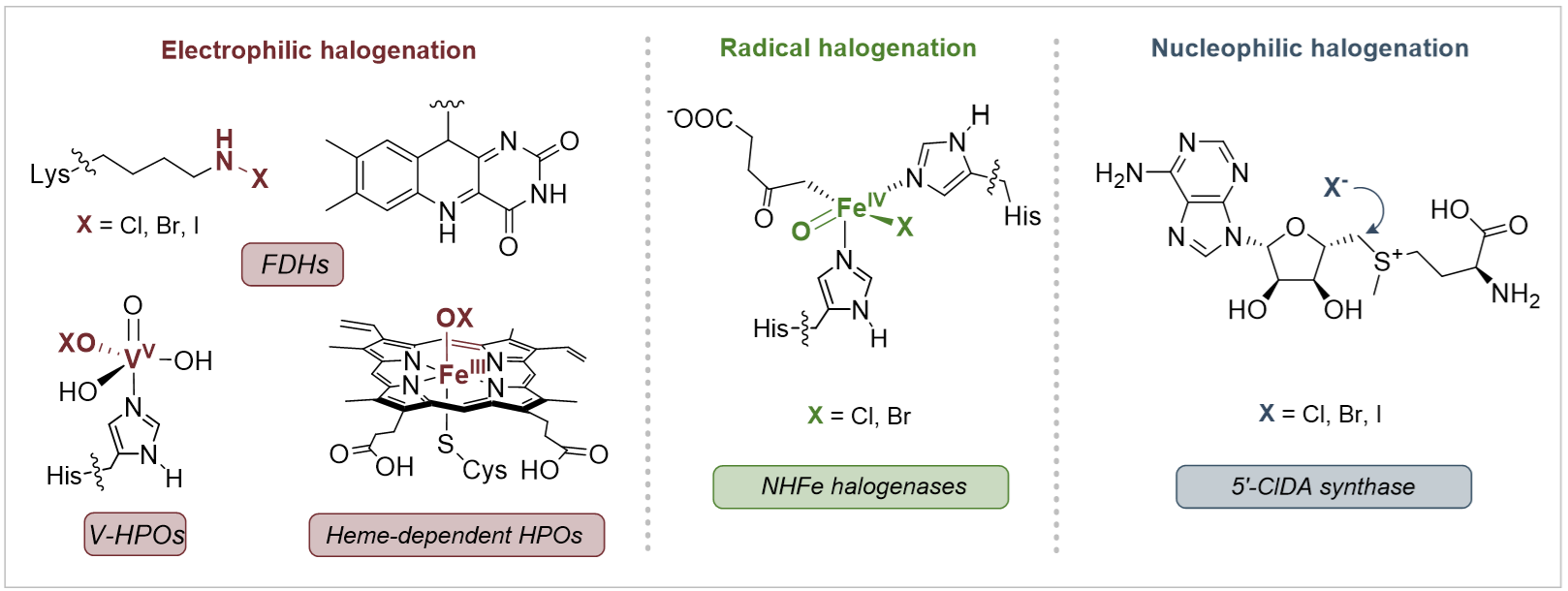
圖1:鹵化酶催化機制
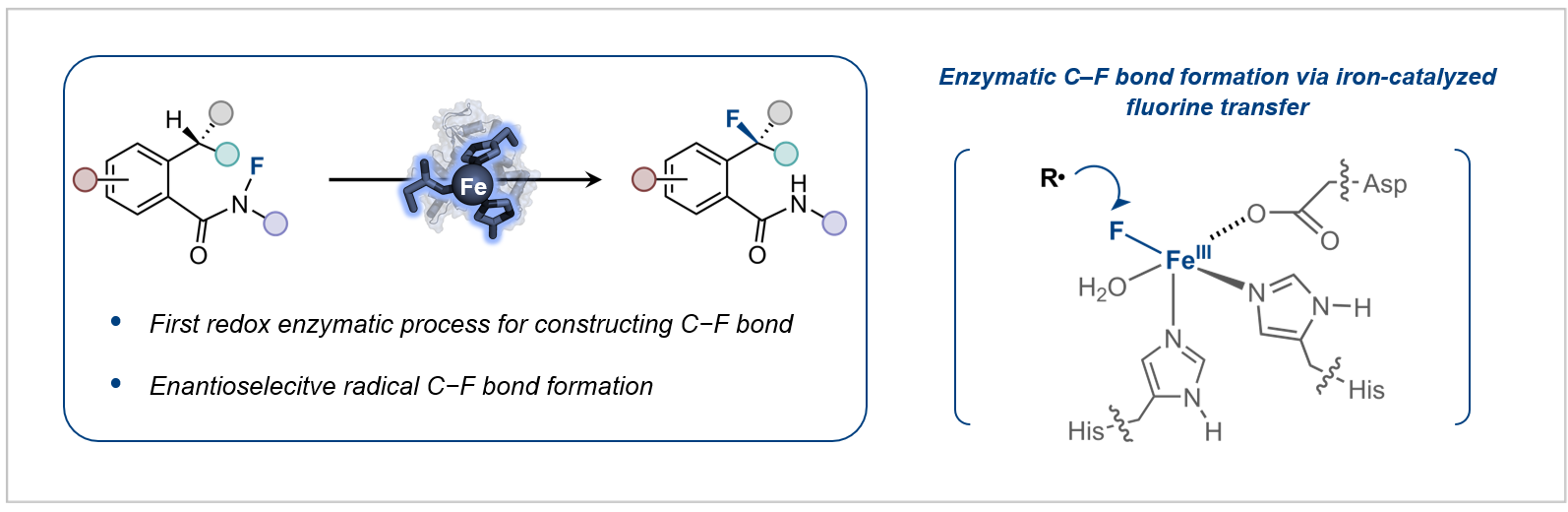
圖2:酶催化不對稱氟轉移反應
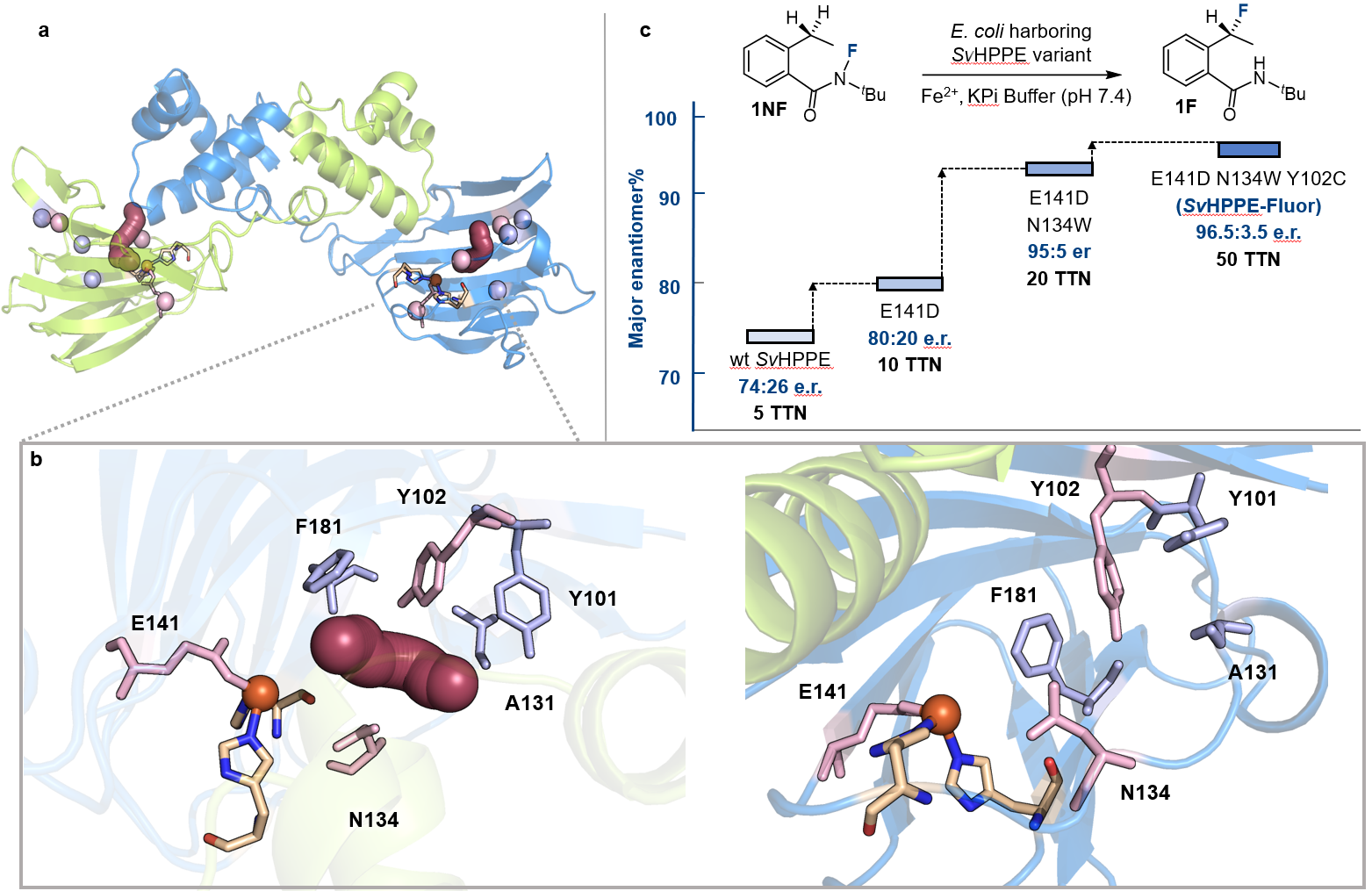
圖3:酶定向進化對反應進行優化
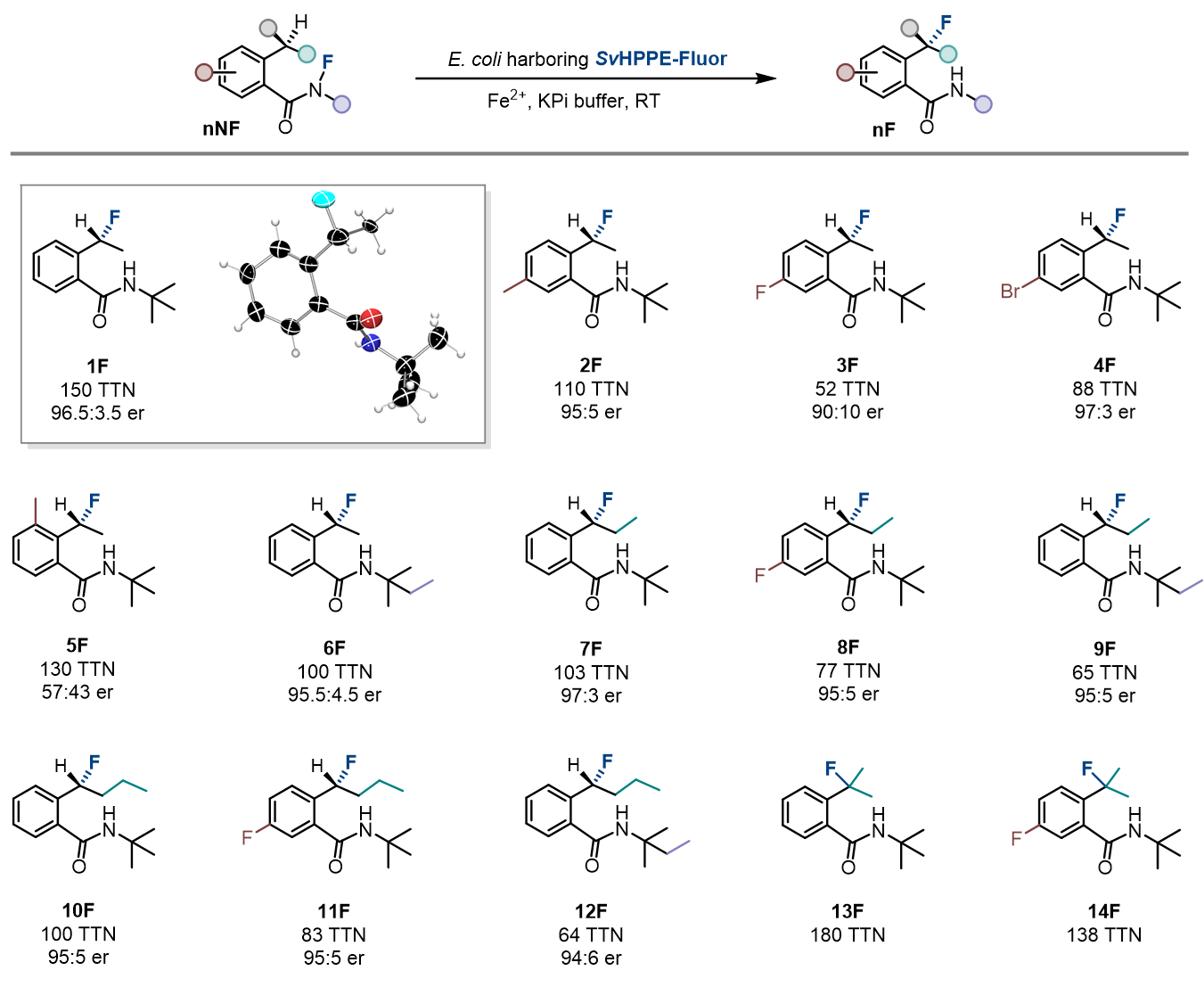
圖4:酶促反應的底物范圍
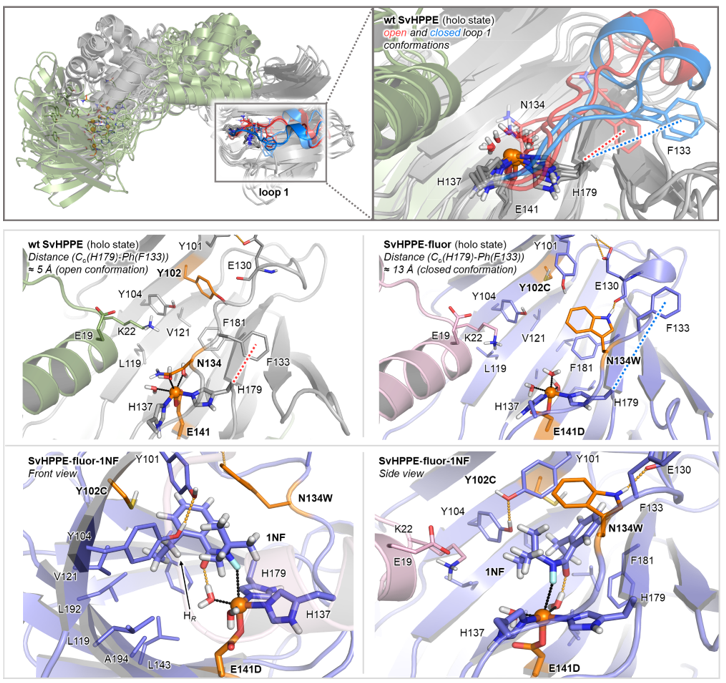
圖5:分子動力學模擬(MD)
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn