




正文
近年來(lái),NHC催化的自由基反應(yīng)取得了顯著進(jìn)展,該研究團(tuán)隊(duì)一直致力于NHC有機(jī)小分子催化的自由基反應(yīng)研究(Nat. Catal. 2024, doi: 10.1038/s41929-024-01194-5; Angew. Chem. Int. Ed. 2022, 61, e202116629; Angew. Chem. Int. Ed. 2022, 61, e202207824; Angew. Chem. Int. Ed. 2020, 59, 1863-1870; Chem. Sci. 2022, 13, 2584-2590; ACS Catal. 2024, 14, 3181-3190.)。盡管NHC催化的自由基反應(yīng)與氫原子遷移(HAT)策略的結(jié)合,已經(jīng)成為開(kāi)發(fā)具有挑戰(zhàn)性化學(xué)反應(yīng)的有力工具。然而除氫原子外,目前尚無(wú)關(guān)于NHC催化介導(dǎo)的其他雜原子基團(tuán)遷移的報(bào)道。本項(xiàng)研究通過(guò)新開(kāi)發(fā)的具有缺電子離去基團(tuán)的β-硼酸酯底物,經(jīng)“單電子還原策略”生成關(guān)鍵的β-硼自由基中間體,隨后通過(guò)1, 2-硼遷移、自由基偶聯(lián)生成一系列β-酰基硼化物。該催化策略同樣適用于藥物分子和活性產(chǎn)物的后期修飾。通過(guò)一系列機(jī)理實(shí)驗(yàn)和密度泛函理論(DFT)計(jì)算,研究了反應(yīng)的初步機(jī)理。
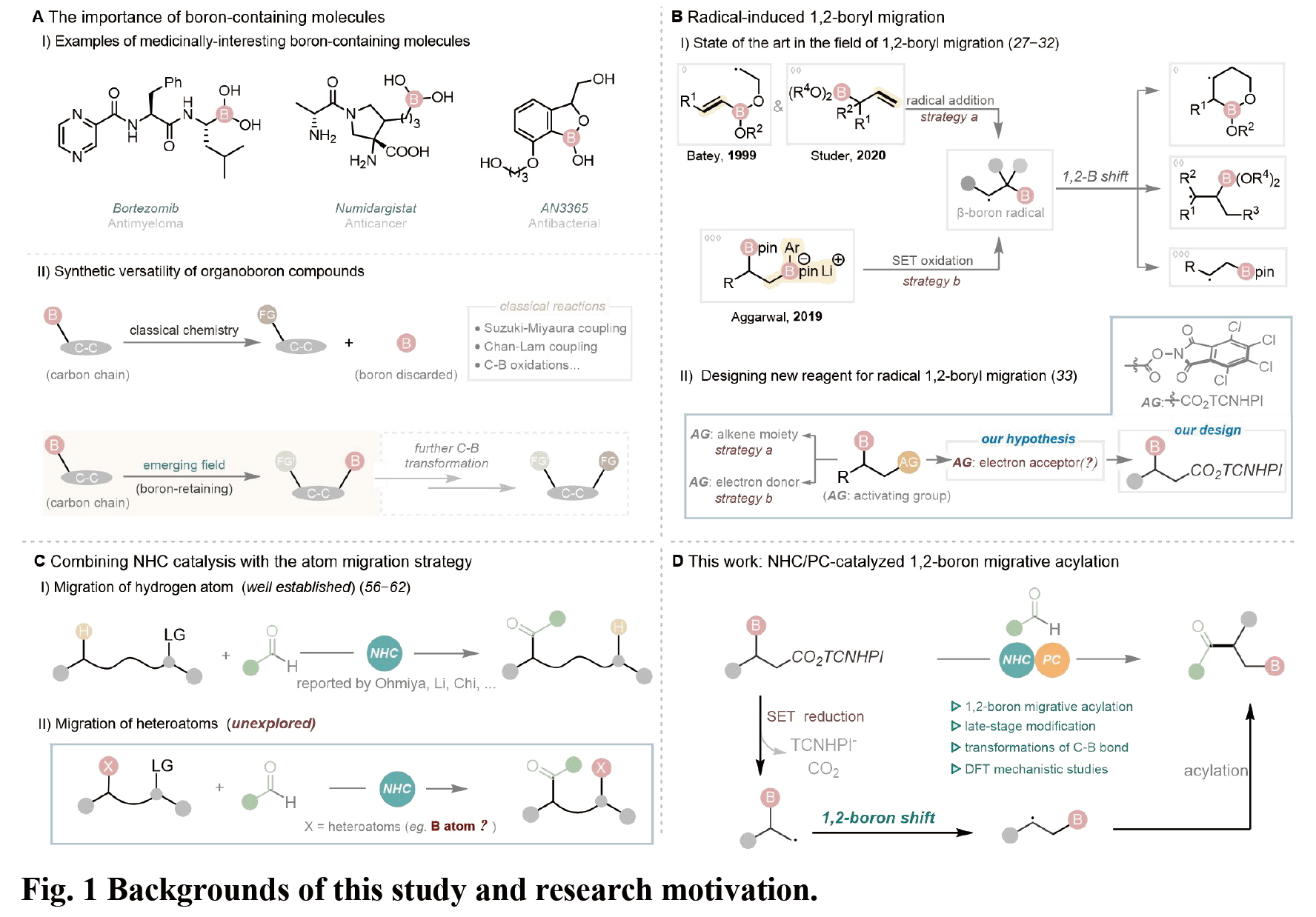
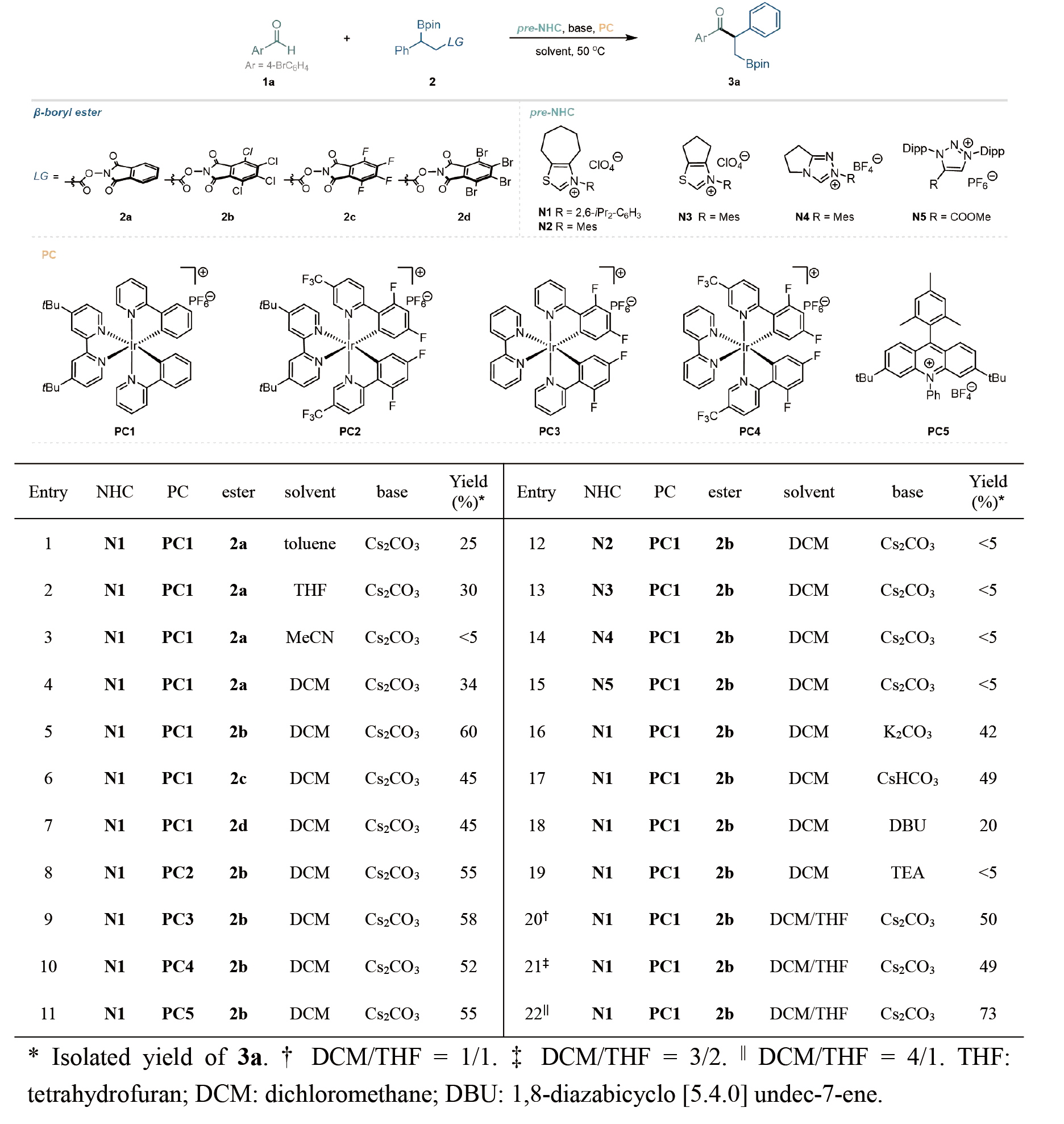
該團(tuán)隊(duì)首先以對(duì)溴苯甲醛1a和β-硼基-N-羥基鄰苯二甲酰亞胺(NHPI)酯2為模型底物,通過(guò)條件篩選結(jié)果表明:以1a和TCNHPI酯2b為底物,PC1為光催化劑,N1為氮雜環(huán)卡賓催化劑,Cs2CO3為堿,二氯甲烷/四氫呋喃(4:1)為溶劑,能夠以73%的產(chǎn)率得到1, 2-硼遷移酰基化產(chǎn)物3a。
Table 1. Optimization studies.
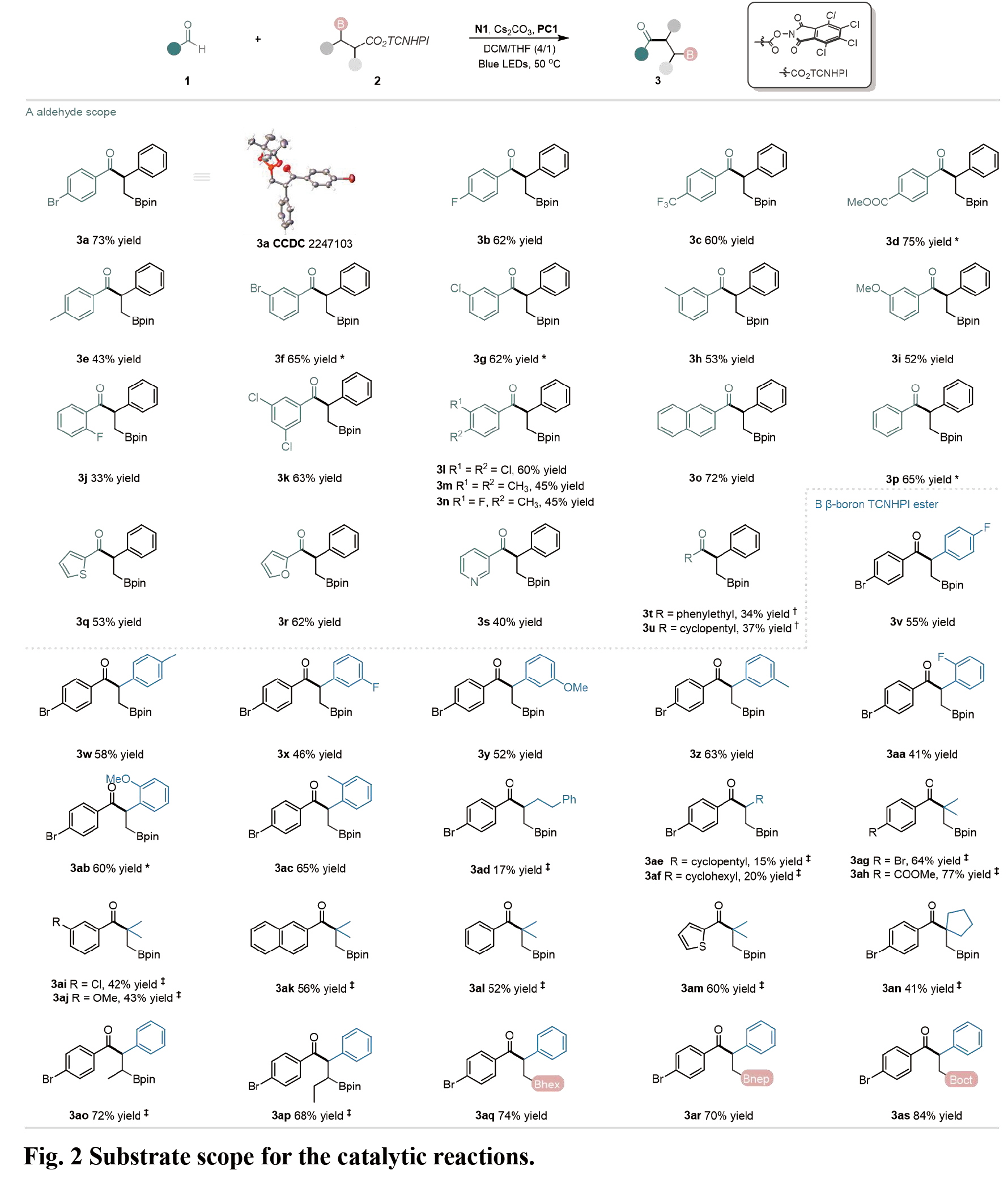
在最優(yōu)條件下,作者對(duì)反應(yīng)的普適性進(jìn)行了考察。對(duì)于醛類(lèi)底物,帶有吸電子或供電子取代基的對(duì)位和間位苯甲醛都能與該催化體系兼容;鄰位取代的苯甲醛反應(yīng)也能順利進(jìn)行;雙取代芳醛、稠環(huán)芳醛和各種雜芳香醛同樣適用該催化體系。以脂肪醛為底物時(shí),反應(yīng)也能順利進(jìn)行。對(duì)于β-硼基TCNHPI酯類(lèi)底物,芳環(huán)的對(duì)位、間位或鄰位引入富電子或缺電子取代基時(shí),該催化體系均能兼容;非芐基的TCNHPI酯底物也能順利參與反應(yīng)。其他硼源(如:Bhex、Bnep、Boct)作為1, 2-硼遷移的基團(tuán)時(shí),同樣能夠得到目標(biāo)產(chǎn)物。
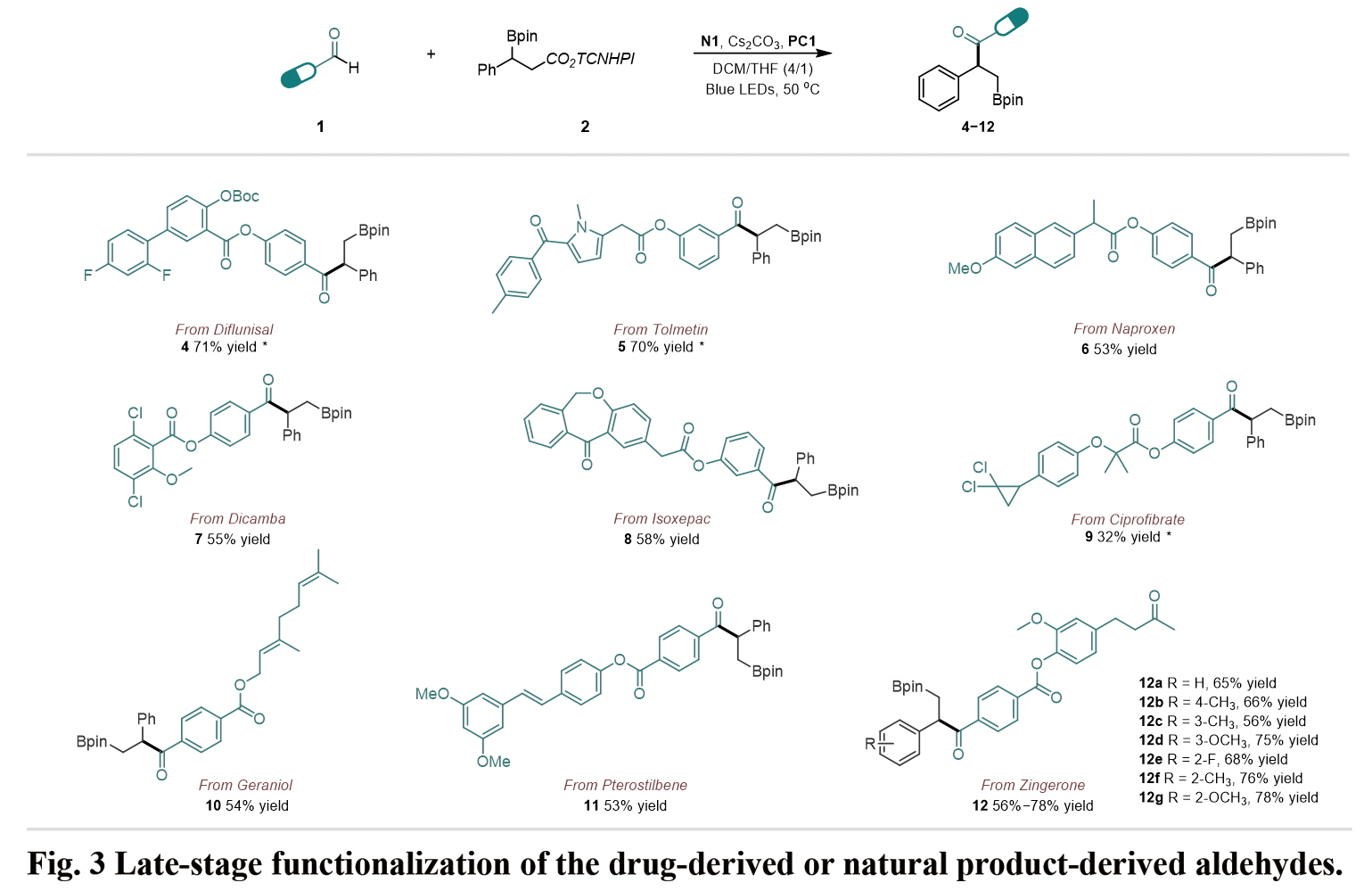
該催化體系反應(yīng)條件溫和,可用于多種藥物骨架和生物活性分子的后期官能化。例如,非甾體類(lèi)抗炎藥二氟尼柳(Diflunisal)、托麥汀(Tolmetin)和萘普生(Naproxen)、降脂類(lèi)藥物環(huán)丙貝特(Ciprofibrate)、以及生物活性分子香葉醇(Geraniol)、紫檀芪(Pterostilbene)、姜酮(Zingerone)等。
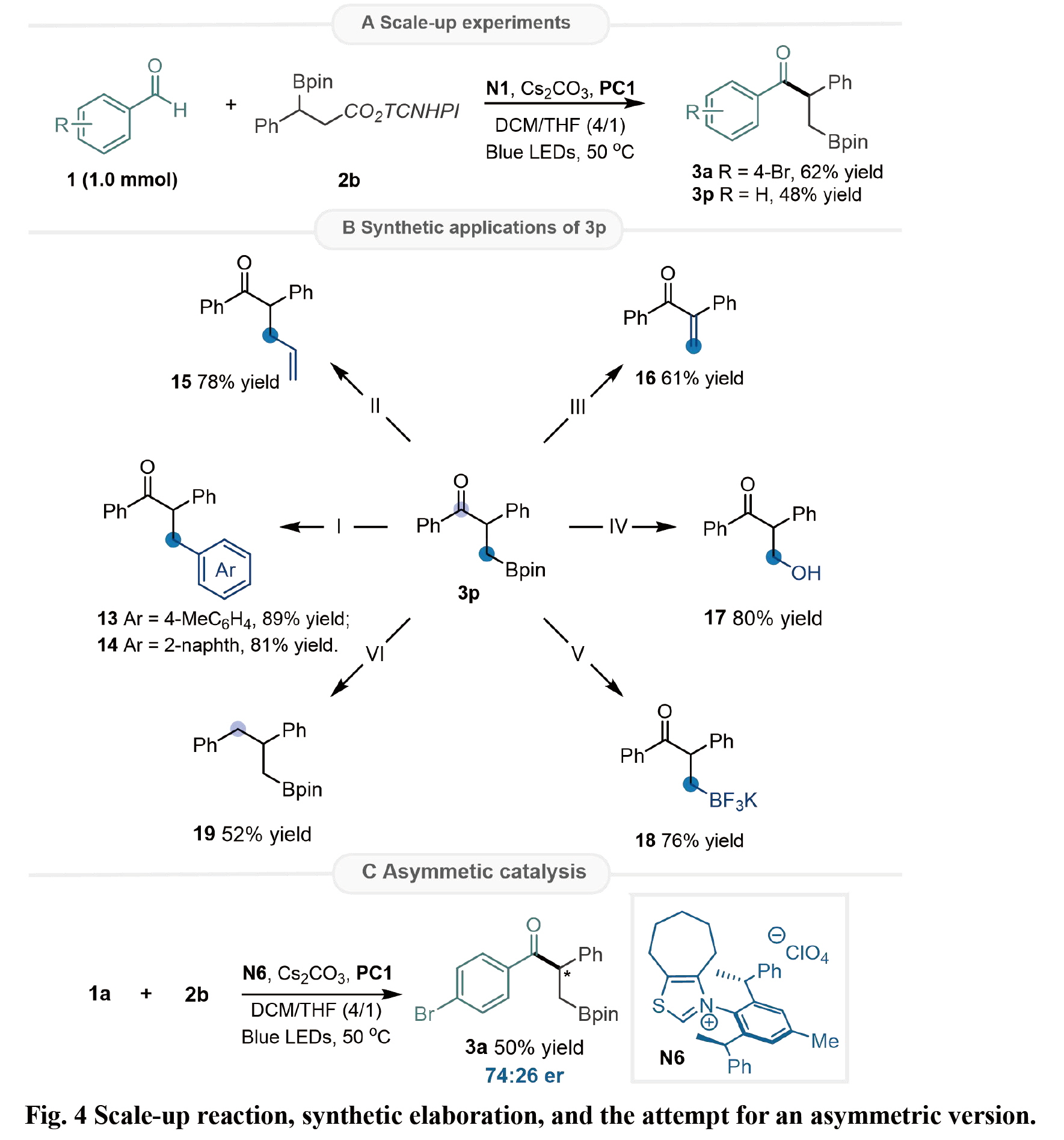
隨后,通過(guò)放大反應(yīng)和對(duì)硼遷移酰化產(chǎn)物的進(jìn)一步轉(zhuǎn)化,成功實(shí)現(xiàn)了含硼化合物向各種官能團(tuán)的衍生化(如偶聯(lián)、乙烯基化、氧化、氟硼酸鉀等),進(jìn)一步證明了有機(jī)硼化合物的有用性。此外,作者利用課題組自主設(shè)計(jì)合成的手性噻唑鎓NHC催化劑N6,對(duì)反應(yīng)的不對(duì)稱(chēng)控制進(jìn)行了初步探索,反應(yīng)能以中等的對(duì)映選擇性得到1, 2-硼遷移酰化產(chǎn)物3a。
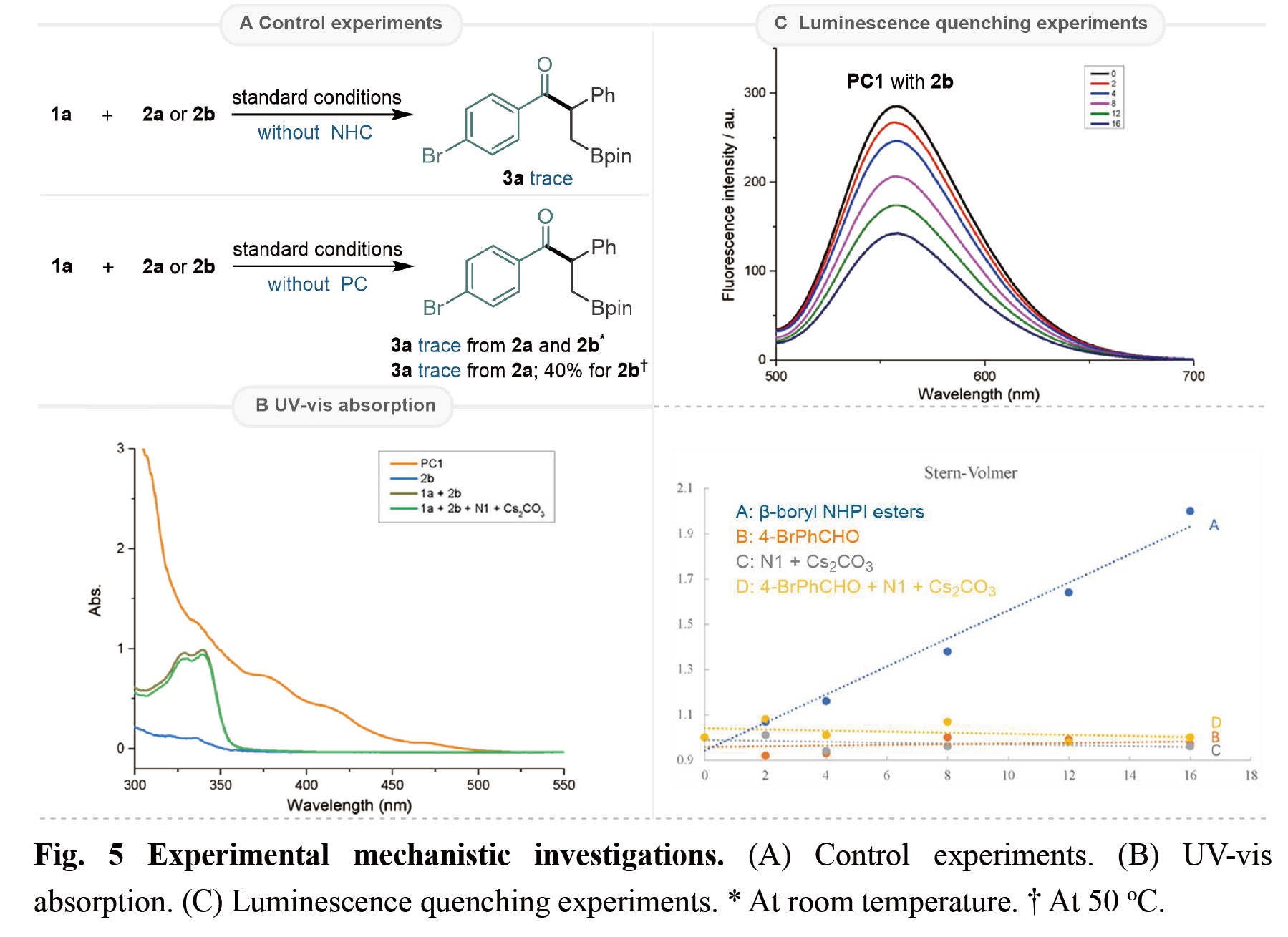
為了闡明該1, 2-硼遷移酰化的反應(yīng)機(jī)理,作者進(jìn)行了詳細(xì)的機(jī)理實(shí)驗(yàn)研究。首先,通過(guò)控制實(shí)驗(yàn)發(fā)現(xiàn),在不使用NHC催化劑的情況下,無(wú)目標(biāo)產(chǎn)物生成。在室溫且沒(méi)有光催化劑和光照的條件下,無(wú)論是以2a還是2b為底物,都無(wú)法生成目標(biāo)產(chǎn)物。在50°C且沒(méi)有光催化劑和光照的條件下,以2a為底物時(shí)沒(méi)有產(chǎn)生任何產(chǎn)物,但以2b為底物時(shí)生成了目標(biāo)產(chǎn)物3a,產(chǎn)率為40%。通過(guò)紫外-可見(jiàn)吸收光譜實(shí)驗(yàn),證實(shí)光催化過(guò)程是由光催化劑的激發(fā)引發(fā)的。熒光淬滅實(shí)驗(yàn)表明,激發(fā)態(tài)的PC1很容易被活性酯2b淬滅。通過(guò)開(kāi)關(guān)燈實(shí)驗(yàn)以及量子產(chǎn)率的測(cè)定,顯示該反應(yīng)是催化自由基過(guò)程。此外,作者測(cè)定了2b的還原電位,表明激發(fā)態(tài)光催化劑與活性酯2b之間的單電子轉(zhuǎn)移是可行的。
為了更深入地理解該催化策略的機(jī)理,作者進(jìn)一步通過(guò)密度泛函理論(DFT)計(jì)算,研究了各反應(yīng)路徑的能量,為光促進(jìn)的NHC催化的自由基誘導(dǎo)的1, 2-硼遷移酰化機(jī)理提供了可靠的依據(jù)。在此基礎(chǔ)上,作者提出了合理的反應(yīng)途徑:首先,光催化劑在光照條件下被激發(fā),隨后被活性酯淬滅,發(fā)生單電子轉(zhuǎn)移,生成烷基自由基IV和相應(yīng)的光催化劑Ir(IV)。接下來(lái),烷基自由基IV通過(guò)1, 2-硼遷移,轉(zhuǎn)化為更穩(wěn)定的自由基V。同時(shí),在堿性條件下,醛與卡賓催化劑I縮合形成去質(zhì)子化的Breslow中間體II。富電子的Breslow中間體II與光催化劑Ir(IV)發(fā)生單電子轉(zhuǎn)移,再生Ir(III)光催化劑,并生成Breslow中間體衍生的酮自由基物種III。另一種可能的途徑是,加熱條件可以促進(jìn)Breslow中間體II和活性酯2之間的直接單電子轉(zhuǎn)移,生成烷基自由基IV,然后轉(zhuǎn)化為更穩(wěn)定的自由基V和酮自由基物種III。酮自由基物種III和自由基V之間發(fā)生自由基-自由基交叉偶聯(lián)。最后,釋放催化劑完成催化循環(huán),同時(shí)生成目標(biāo)產(chǎn)物3。

總結(jié)
聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認(rèn)同其觀點(diǎn)或證實(shí)其描述。若有來(lái)源標(biāo)注錯(cuò)誤或侵犯了您的合法權(quán)益,請(qǐng)作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時(shí)更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn