論文DOI:10.1021/jacs.4c11145
南京大學(xué)俞壽云課題組/天津大學(xué)黨延峰課題組合作報(bào)道了一種光激發(fā)銅催化的非環(huán)狀烯烴對(duì)映選擇性烯丙基C(sp3)–H酰氧基化反應(yīng),高效制備了一類(lèi)手性烯丙基酰氧基化產(chǎn)物。該研究通過(guò)創(chuàng)新的光激發(fā)模式,克服了傳統(tǒng)Kharasch-Sosnovsky反應(yīng)底物適用范圍窄、立體選擇性差的局限。
碳?xì)洌––H)鍵是有機(jī)分子中最常見(jiàn)的結(jié)構(gòu),其直接官能團(tuán)化能夠避免底物預(yù)活化的需求,為目標(biāo)分子的合成提供了更簡(jiǎn)潔高效的途徑。然而,由于C–H鍵,特別是C(sp3)–H鍵的化學(xué)惰性,這類(lèi)分子的選擇性轉(zhuǎn)化,尤其是對(duì)映選擇性的控制,成為了一項(xiàng)極其困難的挑戰(zhàn)。目前,對(duì)不對(duì)稱(chēng)烯丙基C(sp3)–H鍵直接酰氧基化的研究仍十分有限。在Henry和White課題組針對(duì)環(huán)狀烯烴和末端烯烴所做的鈀催化與乙酸的不對(duì)稱(chēng)氧化烯丙基乙酰氧基化反應(yīng)中,盡管取得了一定進(jìn)展,但兩者的對(duì)映選擇性控制均不理想(圖1a)。銅催化的Kharasch-Sosnovsky反應(yīng)是經(jīng)典的烯丙基C–H鍵直接氧化合成烯丙酯的策略,然而其不對(duì)稱(chēng)版本目前僅適用于環(huán)狀烯烴。盡管少數(shù)研究嘗試了非環(huán)烯烴的不對(duì)稱(chēng)Kharasch-Sosnovsky反應(yīng),但效果同樣不夠理想(b/l > 20:1,67% ee,圖1b)。當(dāng)前,不對(duì)稱(chēng)Kharasch-Sosnovsky反應(yīng)仍然存在諸多局限,如反應(yīng)時(shí)間長(zhǎng)、底物范圍狹窄、需大量過(guò)量烯烴以及化學(xué)鍵成鍵類(lèi)型有限等問(wèn)題。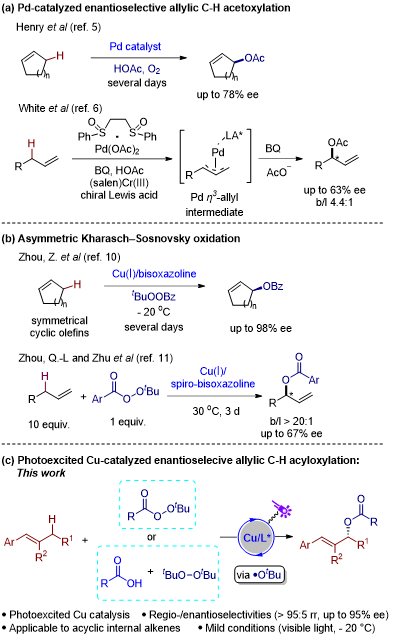
光反應(yīng)作為一種溫和高效的反應(yīng)模式,憑借其獨(dú)特的反應(yīng)性,已成為當(dāng)前研究的熱點(diǎn)。南京大學(xué)俞壽云課題組一直致力于發(fā)展可見(jiàn)光誘導(dǎo)的不對(duì)稱(chēng)催化反應(yīng)研究(J. Am. Chem. Soc. 2022, 144, 10958; ACS Catal. 2023, 13, 2857; Org. Lett. 2024, 26, 5232; J. Am. Chem. Soc. 2024, 146, 21137)。基于此,俞壽云課題組(實(shí)驗(yàn)部分)與天津大學(xué)黨延峰課題組(理論計(jì)算部分)合作,開(kāi)發(fā)了這一新型光激發(fā)銅催化的非環(huán)狀內(nèi)烯的對(duì)映選擇性烯丙基C(sp3)–H酰氧基化反應(yīng)。該反應(yīng)不僅在較溫和的條件下實(shí)現(xiàn)了轉(zhuǎn)化,而且顯著拓寬了此反應(yīng)兼容的底物范圍,成功合成了一類(lèi)具有優(yōu)異對(duì)映選擇性和區(qū)域選擇性的烯丙基C–H氧化產(chǎn)物。DFT計(jì)算為反應(yīng)機(jī)理提供了理論根據(jù)并對(duì)反應(yīng)的高區(qū)域選擇性和對(duì)映選擇性提供了合理解釋。作者首先選用 (E)-β-丙基苯乙烯 (1a) 和過(guò)氧化苯甲酸叔丁酯 (TBPB, 2a) 作為烯丙基 C–H氧化反應(yīng)的模板底物,開(kāi)展反應(yīng)條件篩選(表1)。初始催化體系由 Cu(CH3CN)4PF6(2.0 mol %)和手性雙噁唑啉(Box)配體 L1(2.5 mol %)組成,反應(yīng)組分溶于1.0 mL DCE,在氮?dú)鈿夥障拢褂?5 W藍(lán)色LED燈照射16小時(shí)。結(jié)果顯示,C-H 酰氧基化產(chǎn)物 3a 的GC產(chǎn)率為76%,對(duì)映選擇性良好(81% ee)。經(jīng)過(guò)系統(tǒng)篩選,最終確定了Cu(CH3CN)4PF6和配體L4,以DCE作為溶劑。為提高對(duì)映選擇性,反應(yīng)在-20°C下進(jìn)行,雖然對(duì)映選擇性顯著提升,但產(chǎn)率下降。通過(guò)光源篩選,作者發(fā)現(xiàn)-20°C下使用波長(zhǎng)390 nm的紫色LED燈照射,能夠在不降低產(chǎn)率的情況下獲得優(yōu)異的對(duì)映選擇性(分離收率78%,92% ee)。控制實(shí)驗(yàn)表明,銅配體催化劑和光照都是反應(yīng)所必需的。
表1. 條件篩選
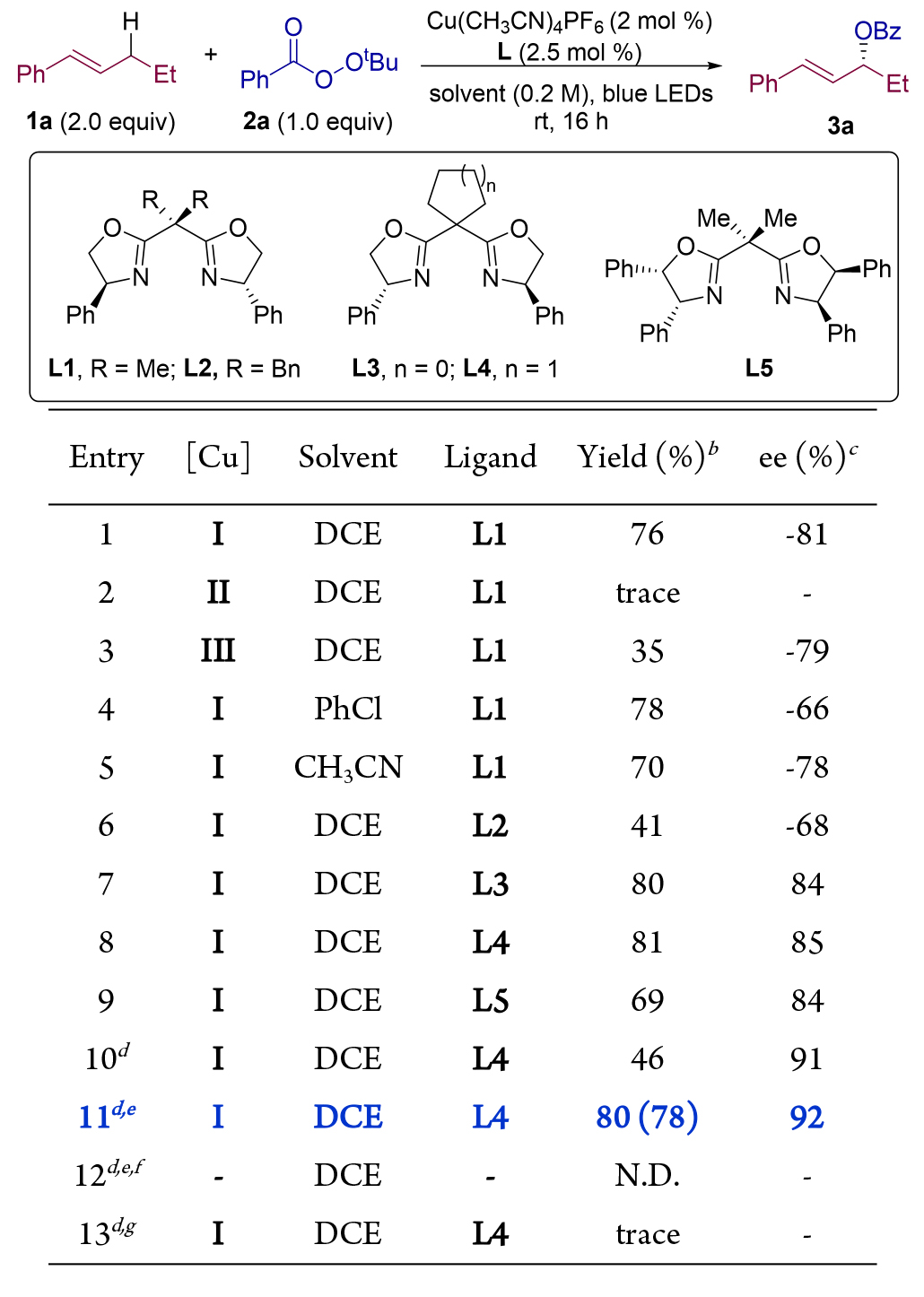
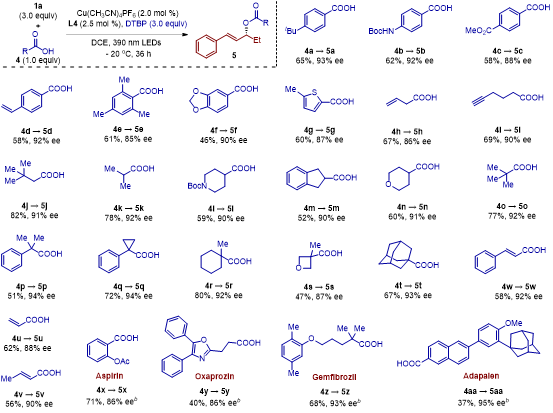
在確定反應(yīng)條件后,作者考察了底物的適用范圍(圖2)。延長(zhǎng)或縮短烷基鏈,均能獲得與模板反應(yīng)相似的產(chǎn)率和對(duì)映選擇性。無(wú)論是鄰位、間位、對(duì)位的給電子或吸電子基團(tuán)以及鹵素取代基,該反應(yīng)都表現(xiàn)出優(yōu)異的區(qū)域選擇性和對(duì)映選擇性。此外,不僅是二取代烯烴,三取代烯烴同樣適用。過(guò)氧化物的底物擴(kuò)展實(shí)驗(yàn)表明,各類(lèi)過(guò)氧化羧酸酯均能很好地參與這一反應(yīng)。
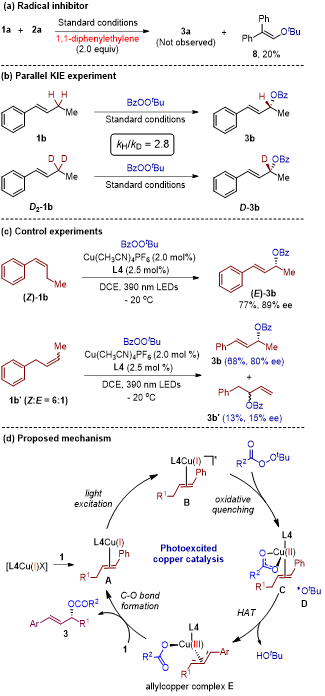
考慮到過(guò)氧化羧酸酯的預(yù)制和苛刻的保存條件,作者進(jìn)一步探討了是否可以使用來(lái)源更廣泛的羧酸作為親核試劑,并額外添加二叔丁基過(guò)氧化物作為氧化劑,進(jìn)行三組分反應(yīng)(圖3)。令人鼓舞的是,當(dāng)作者探索多種商業(yè)可得的羧酸時(shí),目標(biāo)轉(zhuǎn)化依然順利進(jìn)行。如圖3所示,這一策略適用于多種羧酸,包括芳香羧酸、雜芳環(huán)羧酸及多種脂肪類(lèi)羧酸,均能以相當(dāng)?shù)漠a(chǎn)率(37%?82%)和優(yōu)異的對(duì)映選擇性(85%?95% ee)合成相應(yīng)的手性烯丙酯。三組分反應(yīng)的成功極大地拓展了底物適用范圍。為了進(jìn)一步展示該反應(yīng)的合成實(shí)用性,作者對(duì)二組分和三組分反應(yīng)進(jìn)行了克級(jí)放大(圖4)。在放大反應(yīng)中,產(chǎn)率和選擇性均得到了良好的保持。隨后,作者對(duì)手性烯丙酯的酯基和雙鍵進(jìn)行了簡(jiǎn)單的轉(zhuǎn)化,以進(jìn)一步證明該反應(yīng)的應(yīng)用潛力。圖4. 克級(jí)實(shí)驗(yàn)及合成轉(zhuǎn)化最后,作者進(jìn)行了機(jī)理實(shí)驗(yàn)并提出了可能的反應(yīng)機(jī)制(圖5)。最初,L4Cu(I)X配合物與烯烴1結(jié)合,形成活性催化物種Cu(II)-烯烴配合物A。在光激發(fā)下,配合物A轉(zhuǎn)變?yōu)槠浼ぐl(fā)態(tài)B。該激發(fā)配合物B在TBPB的促進(jìn)下經(jīng)歷單電子氧化,生成苯甲酸配合物L4Cu(II)物種C和叔丁氧自由基D。隨后,叔丁氧自由基D與苯甲酸配合物C發(fā)生HAT過(guò)程,形成關(guān)鍵的π-烯丙基Cu(III)中間體E。該中間體E接著經(jīng)歷對(duì)映選擇性還原消除,生成手性烯丙酯3,并再生L4Cu(I)配合物A,進(jìn)入下一個(gè)催化循環(huán)。圖5. 機(jī)理實(shí)驗(yàn)及反應(yīng)可能的機(jī)制為驗(yàn)證提出的反應(yīng)機(jī)理,作者與天津大學(xué)的黨延峰課題組合作進(jìn)行了DFT計(jì)算。以光激發(fā)的L4/Cu催化的不對(duì)稱(chēng)Kharasch-Sosnovsky反應(yīng)(1b與2a的反應(yīng))作為機(jī)理研究的例證。如圖6所示,L4/Cu(I)-π-1b(IM1)在催化反應(yīng)開(kāi)始前被確認(rèn)為最穩(wěn)定的物種,因此設(shè)定為能量曲面的零點(diǎn)。首先,作者考慮了在沒(méi)有光激發(fā)情況下的底物活化。計(jì)算結(jié)果顯示,L4/Cu(I)與TBPB發(fā)生氧化反應(yīng)以激活O?O鍵,從而形成活性苯甲酸復(fù)合物L4/Cu(II)和叔丁氧自由基。然而,這一過(guò)程需要22.0 kcal/mol的能壘,在實(shí)驗(yàn)條件下(-20 °C)無(wú)法達(dá)到,因此排除了此反應(yīng)路徑的可能性。這一計(jì)算結(jié)果與表1中的對(duì)照實(shí)驗(yàn)(條目13)一致,驗(yàn)證了在無(wú)光照情況下僅形成微量產(chǎn)物的結(jié)論。接著,作者探討了銅催化中的光激發(fā)過(guò)程。光氧化還原循環(huán)中電子轉(zhuǎn)移過(guò)程的能量圖如圖6所示。L4/Cu(I)-1b(IM1)被光激發(fā)至IM1S1。IM1S1的振動(dòng)弛豫及隨后發(fā)生的系間竄躍(ISC)導(dǎo)致最低三重態(tài)IM1T1的形成,其熱力學(xué)能量與基態(tài)IM1相比提高了57.2 kcal/mol,從而賦予其更強(qiáng)的氧化還原活性以促進(jìn)后續(xù)反應(yīng)。隨后,IM1T1通過(guò)單電子轉(zhuǎn)移(SET)與TBPB反應(yīng),生成L4/Cu(II)物種IM2和叔丁氧自由基,反應(yīng)的活化自由能ΔGSET?為0.3 kcal/mol,而自由能變化ΔGSET為-57.8 kcal/mol。IM2通過(guò)解離一分子的烯烴1b釋放7.9 kcal/mol的能量,轉(zhuǎn)化為苯甲酸復(fù)合物L4/Cu(II)。叔丁氧自由基通過(guò)HAT(TS1)活化烯丙基C(sp3)–H鍵,僅需8.9 kcal/mol的能壘即可生成烯丙基自由基IM4,該過(guò)程的放熱量高達(dá)28.7 kcal/mol。值得注意的是,IM2中的直接HAT(TS1')也被測(cè)量,但相比于與游離烯烴1b的HAT步驟(TS1),這一過(guò)程不太有利。苯甲酸復(fù)合物L4/Cu(II) IM3捕獲烯丙基自由基,生成關(guān)鍵的π-烯丙基Cu(III)中間體IM5。L4/Cu(III)復(fù)合物通過(guò)六元環(huán)類(lèi)型的還原消除(TS2a)形成C?O鍵,因?yàn)槠洵h(huán)張力較小,該路徑比通過(guò)η1-烯丙基-Cu(III)/L4物種和(η1-苯甲酸鹽)(η1-烯丙基)Cu/L4過(guò)渡態(tài)的路徑更有利。最后,底物-產(chǎn)物交換生成烯丙酯(R)-3b,并再生L4/Cu(I)復(fù)合物IM1。由于C(sp3)–H鍵的活化(TS1)相較于C?O鍵形成(TS2a)的反應(yīng)能壘更高,因此HAT過(guò)程是該反應(yīng)的速率決定步驟,這與動(dòng)力學(xué)同位素效應(yīng)(KIE)實(shí)驗(yàn)(圖5b)一致。綜合整個(gè)反應(yīng)路徑,涉及的SET、底物解離、HAT、自由基捕獲、還原消除及配體交換等步驟均為放熱反應(yīng),從而推動(dòng)反應(yīng)進(jìn)入下一個(gè)催化循環(huán)。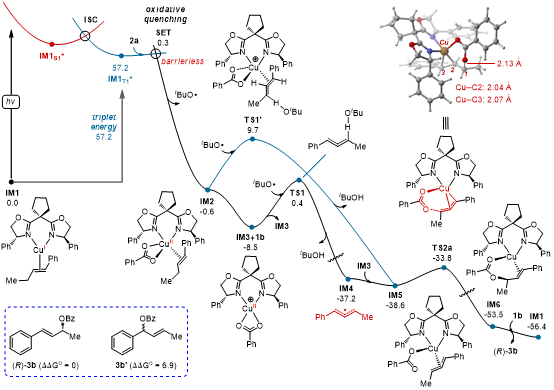 圖6. 光誘導(dǎo)銅催化不對(duì)稱(chēng)Kharasch-Sosnovsky反應(yīng)的自由能曲線(xiàn)圖(單位:kcal/mol)作者在圖7中展示了關(guān)鍵C?O鍵形成過(guò)渡態(tài)的優(yōu)化結(jié)構(gòu)。在四條競(jìng)爭(zhēng)路徑中,生成(R)-3b是最有利的選擇。TS2a的能量至少比TS2a'、TS2b和TS2b'高出1.7 kcal/mol,這一能量差異導(dǎo)致計(jì)算結(jié)果顯示出對(duì)映選擇性和區(qū)域選擇性?xún)A向于(R)-3b,這與實(shí)驗(yàn)結(jié)果相一致。通過(guò)分析異構(gòu)體TS2a和TS2b的結(jié)構(gòu),作者進(jìn)一步理解了它們之間的能量差異,從而解釋了選擇性偏向于(R)-3b而非(S)-3b的原因。在TS2a中,烯丙基苯基團(tuán)朝向遠(yuǎn)離L4的苯基部分,使得配體與底物之間的空間排斥較小。同時(shí),烯丙基上的一個(gè)C?H鍵指向苯環(huán)中心,距離為2.52 ?,這引發(fā)了C?H/π的色散相互作用,從而穩(wěn)定了TS2a。相比之下,在TS2a'中,烯丙基苯基團(tuán)與L4的苯基部分相鄰,導(dǎo)致更強(qiáng)的配體-底物空間排斥(2.53 ?)和較弱的C?H/π色散相互作用(2.86 ?)。這些結(jié)構(gòu)分析揭示了TS2a'更高的能壘,從而解釋了對(duì)映選擇性的來(lái)源。此外,TS2b和TS2b'導(dǎo)致的區(qū)域異構(gòu)體3b'的能量顯著更高,這主要是因?yàn)檫@種類(lèi)型的還原消除削弱了烯丙基底物中苯基與乙烯基之間的共軛效應(yīng),而在TS2a中,共軛效應(yīng)并未受到影響。這一趨勢(shì)與相應(yīng)產(chǎn)物的熱力學(xué)穩(wěn)定性一致(圖6中的3b與3b')。因此,結(jié)合共軛效應(yīng)以及上述空間/色散因素,為反應(yīng)高區(qū)域選擇性和對(duì)映選擇性提供了定性的解釋。圖7. 關(guān)鍵C?O鍵形成過(guò)渡態(tài)的優(yōu)化結(jié)構(gòu),選定的鍵長(zhǎng)以(?)為單位
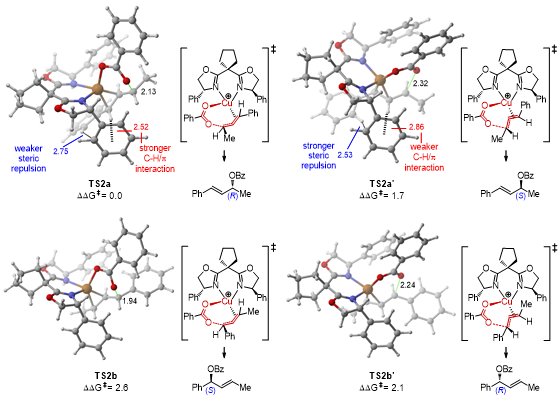
圖6. 光誘導(dǎo)銅催化不對(duì)稱(chēng)Kharasch-Sosnovsky反應(yīng)的自由能曲線(xiàn)圖(單位:kcal/mol)作者在圖7中展示了關(guān)鍵C?O鍵形成過(guò)渡態(tài)的優(yōu)化結(jié)構(gòu)。在四條競(jìng)爭(zhēng)路徑中,生成(R)-3b是最有利的選擇。TS2a的能量至少比TS2a'、TS2b和TS2b'高出1.7 kcal/mol,這一能量差異導(dǎo)致計(jì)算結(jié)果顯示出對(duì)映選擇性和區(qū)域選擇性?xún)A向于(R)-3b,這與實(shí)驗(yàn)結(jié)果相一致。通過(guò)分析異構(gòu)體TS2a和TS2b的結(jié)構(gòu),作者進(jìn)一步理解了它們之間的能量差異,從而解釋了選擇性偏向于(R)-3b而非(S)-3b的原因。在TS2a中,烯丙基苯基團(tuán)朝向遠(yuǎn)離L4的苯基部分,使得配體與底物之間的空間排斥較小。同時(shí),烯丙基上的一個(gè)C?H鍵指向苯環(huán)中心,距離為2.52 ?,這引發(fā)了C?H/π的色散相互作用,從而穩(wěn)定了TS2a。相比之下,在TS2a'中,烯丙基苯基團(tuán)與L4的苯基部分相鄰,導(dǎo)致更強(qiáng)的配體-底物空間排斥(2.53 ?)和較弱的C?H/π色散相互作用(2.86 ?)。這些結(jié)構(gòu)分析揭示了TS2a'更高的能壘,從而解釋了對(duì)映選擇性的來(lái)源。此外,TS2b和TS2b'導(dǎo)致的區(qū)域異構(gòu)體3b'的能量顯著更高,這主要是因?yàn)檫@種類(lèi)型的還原消除削弱了烯丙基底物中苯基與乙烯基之間的共軛效應(yīng),而在TS2a中,共軛效應(yīng)并未受到影響。這一趨勢(shì)與相應(yīng)產(chǎn)物的熱力學(xué)穩(wěn)定性一致(圖6中的3b與3b')。因此,結(jié)合共軛效應(yīng)以及上述空間/色散因素,為反應(yīng)高區(qū)域選擇性和對(duì)映選擇性提供了定性的解釋。圖7. 關(guān)鍵C?O鍵形成過(guò)渡態(tài)的優(yōu)化結(jié)構(gòu),選定的鍵長(zhǎng)以(?)為單位本文報(bào)道了一種光激發(fā)銅催化的非環(huán)狀烯烴對(duì)映選擇性烯丙基C(sp3)–H酰氧基化反應(yīng)。該創(chuàng)新方法克服了以往底物范圍有限、反應(yīng)條件嚴(yán)格和對(duì)映體選擇性不足的挑戰(zhàn)。通過(guò)利用光催化,以及優(yōu)化的銅/雙惡唑啉配合物,實(shí)現(xiàn)了優(yōu)異的反應(yīng)性和出色的區(qū)域、對(duì)映選擇性。廣泛的測(cè)試表明,該方法適用于多種底物,包括各類(lèi)無(wú)環(huán)烯烴和各種過(guò)氧化物(或酸)。同時(shí),反應(yīng)的可擴(kuò)展性得到了驗(yàn)證,能夠在保持高產(chǎn)率和對(duì)映選擇性的同時(shí)進(jìn)行后續(xù)合成修飾。機(jī)理分析表明,TBPB對(duì)激發(fā)態(tài)Cu(I)配合物的單電子氧化是產(chǎn)生叔丁氧自由基和苯甲酸Cu(II)配合物的關(guān)鍵,并進(jìn)一步參與后續(xù)的HAT過(guò)程,形成關(guān)鍵的π-烯丙基Cu(III)中間體。DFT計(jì)算結(jié)果表明,共軛效應(yīng)與空間/色散因子相結(jié)合,為反應(yīng)的高區(qū)域選擇性和對(duì)映選擇性提供了定性和定量解釋。這種激發(fā)態(tài)的過(guò)渡金屬催化模式為未來(lái)其他不對(duì)稱(chēng)光化學(xué)轉(zhuǎn)化以產(chǎn)生對(duì)映體富集的化合物提供了新的機(jī)遇。

俞壽云,教授,博士生導(dǎo)師,化學(xué)化工學(xué)院副院長(zhǎng)。2001年畢業(yè)于南京大學(xué)化學(xué)化工學(xué)院,獲得學(xué)士學(xué)位。同年進(jìn)入中科院上海有機(jī)化學(xué)研究所攻讀博士,師從馬大為研究員,2006年6月獲得博士學(xué)位,并留所任助理研究員。2007年10月至2010年4月,在賓夕法尼亞大學(xué)Jeffrey Bode教授小組進(jìn)行博士后研究。2010年9月,被聘為南京大學(xué)化學(xué)化工學(xué)院副教授,課題組長(zhǎng)。2012年增選為博士生導(dǎo)師,2015年底晉升為教授。主要開(kāi)展不對(duì)稱(chēng)光化學(xué)合成和激發(fā)態(tài)過(guò)渡金屬不對(duì)稱(chēng)催化的研究。獨(dú)立工作以來(lái),以(共同)通訊作者發(fā)表論文100余篇,H-指數(shù)48,已經(jīng)獲得中國(guó)發(fā)明專(zhuān)利授權(quán)4項(xiàng)。擔(dān)任江蘇省化學(xué)化工學(xué)會(huì)第十三屆理事會(huì)理事、《化學(xué)學(xué)報(bào)》和《大學(xué)化學(xué)》編委、Chinese Chemical Letters和《有機(jī)化學(xué)》青年編委。曾獲得寶鋼優(yōu)秀教師獎(jiǎng)(2022)、江蘇省教育成果獎(jiǎng)二等獎(jiǎng)(2021)和Thieme Chemistry Journals Award (2012)等獎(jiǎng)勵(lì)。
課題組鏈接: https://hysz.nju.edu.cn/yusy/
課題組合照